|
Asma
ASMA OCUPACIONAL
As vias aéreas, das fossas nasais aos alvéolos, mantêm contato com 14.000 litros de ar, durante as 40 horas semanais de trabalho, sendo que a atividade física quando presente aumenta a ventilação e expõe o indivíduo a maior concentração de substâncias, que podem alcançar até 12 vezes os níveis de repouso.
A asma é a causa mais comum de doença respiratória relacionada ao trabalho, tendo ultrapassado a asbestose e a silicose, sendo responsável por 1–2% do total de casos.1 Até 10 a 25% dos novos casos de asma em adultos em países altamente industrializados, são atribuíveis a exposições relacionadas ao trabalho.2,3
A prevalência da asma ocupacional (AO) varia em função da profissão e da substância a qual o trabalhador fica exposto. A prevalência pode ser alta como 50% naqueles expostos a enzimas proteolíticas4 e baixa, cerca de 5% em alguns grupos de pacientes expostos a isocianatos5 ou poeira de madeira de cedro.6 As ocupações com os maiores índices de casos novos são os técnicos de pintura de veículos, padeiros e confeiteiros que empregam farinha.
Algumas das causas / exposições mais recentes da AO nos últimos anos incluem uma mistura de ácido peracético e peróxido de hidrogênio, tinta em pó na indústria automotiva, caseína e anidrido piromelítico usado na fabricação de folhas plásticas.7-10 O tempo médio para a suspeita pelo médico de AO é de 2 anos e para o diagnóstico final de 4 anos.11
O prognóstico da AO está amplamente relacionado à gravidade da asma no momento do diagnóstico. Se os trabalhadores permanecerem expostos ao agente causal evoluem para progressivo declínio funcional respiratório, causando obstrução fixa das vias aéreas e limitação ao fluxo aéreo. Em um percentual de 25 a 30% dos pacientes com AO em que a detecção e a remoção completa da exposição ao agente desencadeante é obtida definitivamente ocorre recuperação total, enquanto em 30-35% ocorre diminuição nos sintomas com o tratamento.12 Cerca de um em cada seis pacientes com AO evolui para asma grave.12
Epidemiologia
São poucos os estudos sobre a incidência da AO. Eles são importantes pois a duração dos sintomas varia, o que torna difícil a interpretação da prevalência. Os indivíduos sintomáticos que atribuem seus sintomas à exposição profissional mudam frequentemente de emprego, e muitos mudam inclusive a área de trabalho. As informações disponíveis sobre a incidência de AO provêm da Europa, de dados estatísticos do sistema de compensação previdenciário e de um pequeno número de programas de controle iniciados em diferentes países.
O sistema implantado na Finlândia é o mais antigo, criado em 1923, e talvez o mais completo.13 Os relatórios são emitidos pelo FIOH (Finnish Institute of Occupational Health) baseados em três fontes: médicos pneumologistas, sistema de compensação e companhias de seguros, e casos diagnosticados pelo próprio FIOH. Como as companhias de seguros exigem provas irrefutáveis, o diagnóstico de AO e sua ligação aos agentes causais são geralmente bem estabelecidos.
No Reino Unido, as informações são provenientes de uma fonte oficial e de dois programas voluntários iniciados em 1989: os programas SHIELD da região de West Midlands14 e SWORD (Surveillance of Work-related and Occupational Respiratory Disease).15 O projeto SWORD é baseado em notificações de novos casos de asma por pneumologistas e médicos do trabalho do Reino Unido. Os critérios de diagnóstico não são específicos: os participantes devem relatar todos os casos de doença respiratória que julguem ser devido à exposição no trabalho. O sistema de compensação cobre somente 23 agentes, sendo que em 1993 uma categoria "aberta" foi introduzida.
O sistema adotado pelos Estados Unidos é diferente dos sistemas europeus. O programa SENSOR (Sentinel Event Notification System for Occupational Risks)16 não visa à obtenção de índices epidemiológicos e sim à identificação de casos sentinelas potencialmente perigosos, em vista de uma intervenção investigativa e preventiva sobre o local de trabalho. Os critérios para o diagnóstico são precisos: a asma deve ser diagnosticada por um médico e a associação asma/trabalho deve ser demonstrada. Além disso, o agente implicado deve ser conhecido por sua associação com a asma ou por ser capaz de provocar piora da função pulmonar ou aumento da responsividade brônquica.
Na França, as primeiras informações epidemiológicas sobre a AO foram coletadas somente em 1993, quando de uma pesquisa efetuada através de um questionário realizado com todos os médicos do trabalho pela Sociedade Francesa de Medicina do Trabalho e pela Associação da Asma.17 Em 1996 a Sociedade de Pneumologia de Língua Francesa e a Sociedade Francesa de Medicina do Trabalho criaram o ONAP (Observatoire National des Asthmes Professionnels) inspirado no programa britânico SWORD.15 Nos anos de 1996 e 1997 o ONAP computou cerca de 1.000 fichas de avaliação de AO (704 homens e 368 mulheres) obtidas através de notificações de serviços hospitalares (18%), profissionais liberais (9%), médicos do trabalho (12%), especialistas em patologias profissionais (54%) e outros (4%). Dentre estas fichas, 854 (80,5%) eram casos típicos de AO, 52 (4,9%) casos de síndrome de disfunção reativa das vias aéreas — hoje conhecida como Asma Induzida por Irritantes — e 155 (14,6%) de síndromes asmáticas atípicas. Para o ano de 1996 o ONAP recenseou 394 novos casos de asma profissional sendo a incidência desta patologia neste ano de 17:1.000.000 de trabalhadores.
Em 2019, na Grã-Bretanha ocorreram 198 novos casos de AO relatados pelo SWORD.18 A notificação de novos casos em 2020 foi interrompida pela pandemia de coronavírus. Casos diagnosticados por especialistas relatados via SWORD provavelmente subestimam a verdadeira escala da asma ocupacional.18
Na Alemanha, todas as empresas são obrigatoriamente filiadas a Berufsgenossenschaft, um organismo público legislativo.19 Desta forma, todos os trabalhadores, assalariados e também os autônomos, estão protegidos pela lei. Dentre as finalidades da Berufsgenossenschaft temos: prevenção de acidentes e doenças do trabalho, controle de riscos para a saúde no local de trabalho, tratamento, reabilitação e compensação e auxílio-doença. Três categorias de doenças obstrutivas profissionais são reconhecidas: causadas por sensibilizantes, por irritantes químicos e tóxicos, e as secundárias à exposição de isocianatos, classificadas separadamente.
Classificação e Diagnóstico
A asma ocupacional é definida como uma doença caracterizada por limitação variável ao fluxo aéreo e/ou hiper-responsividade das vias aéreas devido a causas e condições atribuíveis a um ambiente específico e não a estímulos encontrados fora do local de trabalho.20
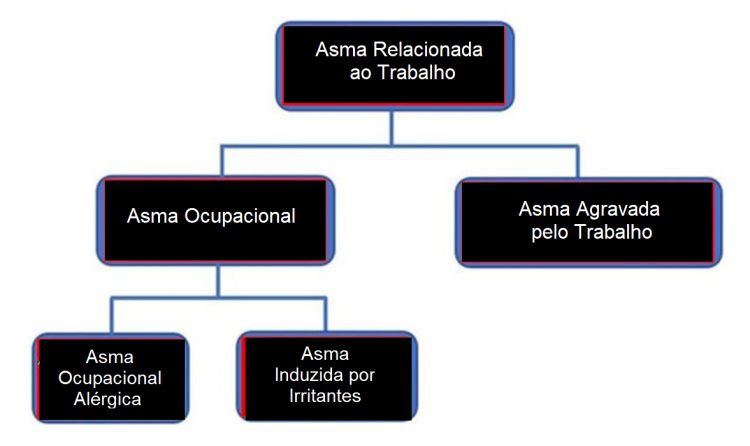
A Asma Relacionada ao Trabalho (ART) pode ser classificada em três fenótipos de acordo com o conhecimento da etiologia e fisiopatologia (Tabela 1): asma agravada pelo trabalho, asma ocupacional alérgica devido à sensibilização e asma induzida por irritantes.
Tabela 1 Tipos de Asma Relacionadas ao Trabalho
A Asma Relacionada ao Trabalho (ART) pode ser diagnosticada em pacientes com asma preexistente ou concomitante, que não se iniciou por exposição ao local do trabalho, porém torna-se pior pelo ambiente ocupacional. Manifesta-se por exacerbação de asma previamente subclínica ou em remissão. Inclui a asma desencadeada por irritantes, como o ar frio ou o exercício intenso ou a exposição a vapores, poeiras e gases. A ART é uma entidade relativamente frequente, atingindo cerca de 20 a 25% dos trabalhadores asmáticos.21-23
Vários são os fatores que predispõem a asma agravada pelo trabalho:
■ Fatores ligados ao local do trabalho exposição a substâncias químicas e suas concentrações; não observância das condutas de segurança; má higiene industrial;
■ Variantes climáticas altos níveis de poluentes oxidantes; inversões térmicas; condições do vento; alérgenos sazonais;
■ Fatores genéticos polimorfismo alélico associado à atopia;
■ Fumo - tabagismo e outras drogas como a maconha cujo consumo, mesmo de alguns poucos cigarros, pode causar severo dano epitelial e o crack;
■ Infecções respiratórias – virais, Clamydia ou Mycoplasma, sinusites infecciosas;
■ Hiper-responsividade brônquica não específica;
■ Diversos – sensibilidade à aspirina, refluxo gastresofágico, efeitos adversos de certos medicamentos como inibidores da ECA e ß-bloqueadores.
A Asma Ocupacional (AO) é definida como uma limitação variável ao fluxo aéreo e/ou hiper-responsividade brônquica não específica, causada por inflamação aguda ou crônica, relacionada à inalação de alérgenos de origem biológica, poeiras, gases, vapores ou fumaças, no ambiente de trabalho.24,25 Divide-se em dois subtipos distintos:26
➭ Asma Alérgica Ocupacional e;
➭ Asma Induzida por Irritantes (AII)
Até o momento existem > 400 substâncias implicadas na asma ocupacional,14 relacionadas a 140 tipos diferentes de atividade profissional, e que podem ser encontradas no portal da Canadian Center for Occupational Health and Safety ou através da publicação inglesa mais antiga  Asthmagen do Health and Safety Executive (HSE). Asthmagen do Health and Safety Executive (HSE).
As principais categorias de agentes relacionadas englobam: antígenos animais, insetos, fungos, plantas, gomas vegetais, enzimas biológicas, anidridos ácidos, aldeídos, isocianatos, aminas alifáticas, aminas aromáticas, metais, drogas farmacêuticas e outras substâncias químicas.14
Estas substâncias podem ser divididas em duas categorias de acordo com o mecanismo de ação: imunológicas (asma alérgica ocupacional) e não imunológicas. As imunológicas podem ser dependentes ou não da mediação pela IgE. As não imunológicas compõem a asma induzida por irritantes.
A asma de causa imunológica (asma com latência) apresenta um período assintomático entre a exposição e o início da sintomatologia respiratória, variando de semanas a 30 anos.27
Ela abrange a AO causada pela maioria dos agentes de Alto Peso Molecular (APM) e alguns de Baixo Peso Molecular (BPM), para os quais foi comprovado um mecanismo mediado pela IgE, e a AO induzida por alguns agentes específicos de BPM nos quais os mecanismos alérgicos responsáveis ainda não foram totalmente caracterizados. A asma de causa imunológica é o tipo mais comum de AO, respondendo por mais de 90% dos casos. Na Tabela 2 as causas mais frequentes relacionadas à asma ocupacional, de acordo com o peso molecular.
Cerca de 40% dos pacientes desenvolvem os sintomas nos dois primeiros anos de exposição, enquanto em 20% os sintomas ocorrem após 10 anos.27 A duração do período de latência pode ser curto, como alguns meses (ou semanas em raras instâncias), ou longo, muitos anos, como visto p. ex. na asma por exposição à poeira da farinha. O risco de desenvolver asma é maior após um ano do início de rinite ocupacional. A atopia aumenta o risco de desenvolver AO causada por exposição a muitos agentes com APM.
O paciente passa a relatar tosse, opressão torácica e sibilos após chegar ao local de trabalho, especialmente após o fim de semana. É a chamada "asma da segunda-feira". Embora a suscetibilidade individual desempenhe um papel importante, o principal fator de risco para o desenvolvimento da AO é o nível de exposição ao alérgeno no local de trabalho.
Durante o período de latência, os alérgenos são processados pelas células dendríticas e macrófagos, que apresentam os antígenos aos linfócitos T auxiliares, os quais estimulam os linfócitos B a produzirem IgE específica. Quando ocorre a reação antígeno-IgE específica nos mastócitos, mediadores químicos são ativados, desencadeando a cascata de eventos inflamatórios. Ocorrendo sensibilização ao agente causal, inicia-se também a resposta inflamatória mediada via linfócitos TH2. Anticorpos IgE específicos são detectados no soro ou através de testes cutâneos na maioria dos casos de asma com latência, desencadeada por proteínas biológicas de APM (5 quilodáltons ou mais), como partículas de produtos de madeira, grãos, têxteis ou látex. Substâncias com BPM (menos de 1 quilodálton) podem causar sensibilização sem, entretanto, produzir IgE específica (isocianatos, cedro ou resinas de acrílico), pois outros mecanismos podem estar envolvidos como anticorpos IgG, e a hipersensibilidade celular mediada. Pacientes com história de atopia e tabagismo são mais suscetíveis a desenvolver resposta a antígenos de APM.
O manejo adequado de um paciente no qual se suspeita de AO implica o estabelecimento de um diagnóstico definido. A primeira medida a ser adotada é a remoção da pessoa afetada do ambiente de trabalho, e iniciar pesquisas para se identificar o agente desencadeante, realizar investigações clínicas e imunológicas apropriadas para se diagnosticar a doença. Pacientes asmáticos sintomáticos em empregos de alto risco e aqueles que relatam melhora fora do trabalho devem ser encaminhados o mais rápido possível para avaliação especializada (quando possível, diretamente para um serviço especializado em doenças pulmonares ocupacionais). Quando, entretanto, o paciente já deixou o emprego que possa ter causado a sua asma o diagnóstico dependerá de uma história clínica ocupacional detalhada, provas de função respiratória e da identificação de sensibilização específica.
O mecanismo da asma ocupacional alérgica, causada por substâncias de APM, é uma reação do tipo I mediada pela IgE, semelhante ao observado na rinite alérgica. Portanto, os testes cutâneos – prick test ou os testes para determinação da IgE específica podem ser utilizados na investigação da AO causada por agentes de APM. No entanto, uma resposta positiva ao teste cutâneo apenas confirma a exposição e sensibilização. Alguns indivíduos podem reagir positivamente ao teste cutâneo e não demonstrar asma induzida por alérgenos.
Poucos são os extratos para alérgenos ocupacionais que estão disponíveis comercialmente, sendo que a maioria não é padronizada, e alguns dos extratos disponíveis podem não ter potência e confiabilidade adequadas.28
O teste cutâneo não avalia adequadamente a resposta aos antígenos de BPM. Assim, os testes cutâneos são inúteis para a maioria dos agentes de BPM, mas são boas ferramentas de diagnóstico para se avaliar trabalhadores sensibilizados a sais complexos de platina e, em alguns casos, em pacientes expostos a outros sais metálicos29 e a persulfatos.
Também é possível usar testes in vitro, como o teste RAST (radioallergosorbent) ou ELISA (enzyme-linked immunoassay), para a detecção de anticorpos IgE específicos para alérgenos. No entanto, os testes cutâneos são geralmente mais sensíveis à detecção precoce da sensibilização do que os testes in vitro. Em algumas circunstâncias, a especificidade das medidas da IgE para agentes ocupacionais pode ser dificultada por reatividades cruzadas alergênicas com aeroalérgenos comuns ou panalérgenos como a profilina.30
Pacientes com suspeita de AO devem efetuar espirometria e monitorização do Pico de Fluxo Expiratório (PFE) que é um instrumento muito útil, porém em muitos casos não é suficientemente sensível – de 75–82% ou específico de 79–88%
a não ser que o paciente ainda esteja exposto ao potencial agente causal e, portanto, exige aferições durante o período trabalho e fora dele.12 Preconiza-se pelo menos uma análise por três semanas, com quatro aferições diárias. O período de 21 dias será dividido por três séries de dias de trabalho com três períodos de afastamento.
O método de excelência para a confirmação do diagnóstico é o teste de provocação específico por inalação em laboratório ou no próprio local de trabalho, que deve ser efetuado sob supervisão de um médico habilitado para execução destes exames.
A ausência de hiper-responsividade brônquica quando o paciente trabalha há pelo menos duas semanas praticamente exclui a AO.
Vandenplas et al.31 estudaram uma grande coorte multicêntrica internacional e retrospectiva (E-PHOCAS) de 1180 indivíduos com diagnóstico de AO com base em resultados positivos de testes de provocação específicos por inalação. No grupo estudado 635 (53,8%) eram de produtos químicos de BPM, 544 (46,1%) por proteínas de APM, enquanto em 13 indivíduos o agente causal não foi identificado. Indivíduos com AO causada por agentes de APM, em comparação com agentes de BPM, eram um pouco mais jovens, mais atópicos, nunca fumaram e, com maior frequência relatavam rinite, conjuntivite e crises de asma mais precoces relacionadas ao trabalho. Por outro lado, a AO por agentes de BPM estava associada à opressão torácica, expectoração diária e crises de asma tardias. Aqueles com AO causada por agentes de APM com maior frequência apresentaram eosinofilia no sangue periférico (> 300 células/mm3) e a fração exalada de óxido nítrico (FeNO) estava mais elevada após a provocação do que em indivíduos com AO por agentes de BPM. Indivíduos com AO causada por agentes de BPM tiveram uma taxa significativamente maior (26%) de exacerbações de asma severa, quando expostos no trabalho, do que os indivíduos sensibilizados a agentes de APM (19%), sendo que estes apresentaram maior risco de inflamação das vias aéreas.
Quando a AO é diagnosticada e o indivíduo continua exposto ao alérgeno de origem, os sintomas tornam-se mais severos e frequentes, inclusive fora do local de trabalho, podendo ser desencadeada também por outros alérgenos ambientais (fumaças do cigarro, perfumes, dióxido de enxofre). Quando afastado do trabalho, livre da exposição ao agente causal, cerca de 60 a 80% dos trabalhadores sensibilizados continuarão a apresentar sintomas, sendo, entretanto, em proporção menor do que nos que continuam sob exposição.
A asma de causa não imunológica é menos comum e não apresenta o período de latência, nem sensibilização. A AII, previamente chamada de Síndrome da Disfunção Reativa das Vias A éreas (RADS), foi descrita por Brooks32,33 em 1985. Foram descritos dez casos de indivíduos que desenvolveram sintomas de asma após uma única exposição, geralmente acidental ou quando de situação em que ocorria pouca ventilação com altos níveis de exposição a vapores, fumaça ou gases irritantes (Tabela 3), sem que nenhum apresentasse história prévia de sintomas respiratórios. A sintomatologia da asma persistiu em média por três meses. O tempo de exposição ao agente variou de alguns minutos até 12 horas (média de 9 h). Outra característica é que a reexposição ao agente não reproduzia a doença.
Tabela 3 Agentes Industriais que Mais Causam a Asma Induzida por Irritantes
Agentes Industriais que Mais Causam Asma Induzida por Irritantes |
Ácido Sulfúrico |
Ácido Fosfórico |
Gás Cloro |
Ácido Clorídrico |
Fosgênio |
Gás Sulfídrico |
Inalação de Fumaças |
Amônia Anidra |
Ácido Acético |
2-Dietilaminoetanolamina |
Cloreto de Zinco |
Vapores de Solda |
Sulfato de Hidrogênio |
Gás Lacrimogênio |
Hidróxido de Sódio |
Silicone |
Impermeabilizantes |
Exaustão Diesel |
Alvejantes (hipoclorito de Cálcio) |
Diisocianato de Tolueno |
O American College of Chest Physician (ACCP)32,26 através do Consenso sobre "Diagnóstico e tratamento da asma relacionada ao trabalho" propôs como critérios para a RADS:
■ Ausência de transtorno respiratório prévio, sintomas de asma ou história de asma em remissão ou condições que possam simular asma
■ A crise de asma ocorre após uma única exposição ou acidente
■ Exposição a altas concentrações de gases, fumaças ou vapores, com propriedades irritantes
■ O início dos sintomas da asma se manifesta dentro de minutos a horas e < 24 h após a exposição
■ Um resultado positivo utilizando o teste de broncoprovocação à metacolina ou teste equivalente, o que significa vias aéreas hiper-responsivas após a exposição
■ Presença de obstrução das vias aéreas, comprovada ou não por provas de função respiratória
■ Descartar a possibilidade de qualquer outra doença pulmonar que explique os sintomas e achados
Prospectivamente, evidenciou-se que em certos pacientes um quadro semelhante ocorria após múltiplas exposições a irritantes e o termo asma induzida por irritantes passou a ser preferido por especialistas. Uma grande variedade de agentes desencadeia a asma induzida por irritantes como poeiras, álcalis, amônia, fumaças, SO2, produtos de limpeza, aldeídos, combustíveis etc. Os pacientes não demonstram sensibilização específica e não apresentam necessariamente testes de provocação positivos.
A patogênese da síndrome não está ainda determinada. Acredita-se que ocorra grave lesão epitelial da mucosa com destruição, por inalação de alta concentração do agente químico, seguida de inflamação neurogênica via reflexos axonais. Ativação de macrófagos e degranulação de mastócitos (não alérgica) podem ocorrer, recrutando células inflamatórias para o local. O quadro histopatológico é de exuberante espessamento da membrana basal, com edema proeminente, com inflamação paucicelular. Os eosinófilos estão esporadicamente presentes e podem ser raramente visualizados através da microscopia ótica convencional, porém podem ser demonstrados por imuno-histoquímica.
Ao contrário dos pacientes com AO imunológica, aqueles com AII, podem, muitas vezes, continuar no mesmo posto de trabalho, caso medidas sejam tomadas para reduzir o risco de acidente similar, assegurando o controle ambiental com a redução dos níveis de irritantes no ar e obviamente, certificando-se de que a asma do trabalhador tenha sido convenientemente tratada e controlada. O tratamento da AII aguda é feito com a medicação habitual para a asma, incluindo corticoides inalatórios e broncodilatadores. Um follow-up destes trabalhadores se faz necessário para se certificar de que a sensibilização não tenha ocorrido, principalmente quando se trata de potentes sensibilizantes como os isocianatos.34,35 Evidências sugerem, no entanto, uma gama de respostas, desde a resolução completa até a incapacidade respiratória persistente.8,36,37
Síndromes Variantes
Bronquite Eosinofílica — Gibson et al.38 descreveram um grupo de pacientes com tosse crônica sem causa aparente, com aumento de eosinófilos e mastócitos no escarro. Estes pacientes não apresentavam obstrução aérea variável, nem hiper-responsividade brônquica inespecífica. Esta nova entidade passou a ser chamada de bronquite eosinofílica. O padrão inflamatório da submucosa das vias aéreas é semelhante ao de pacientes com asma sintomática, achado que foi confirmado por broncoscopia. Vários casos de bronquite eosinofílica relacionados a agentes ocupacionais têm sido descritos.39-42 Nestes casos, a exposição ao acrílico, látex (luvas), esporos de cogumelos, resina epóxi, resultaram em intensa eosinofilia no escarro, sem que houvesse hiper-responsividade e aumento da resistência das vias aéreas.
Potroom Asthma — Relacionada à ocorrência de sintomas de asma entre os trabalhadores da indústria de alumínio.43 A redução eletroquímica do alumínio (conversão da alumina (Al2O3) para alumínio metálico) requer grande quantidade de corrente contínua, que flui através de uma série de células eletrolíticas ou potes". Neste processo, ocorrem grandes emanações de CO2. Se o processo se torna instável são gerados gases de estufa. Sulfatos de alumínio e fluoretos de hidrogênio usados durante o processo de extração eletrolítica do alumínio também são tóxicos e apresentam papel relevante no desenvolvimento dos sintomas crônicos. Além do efeito irritante destes poluentes é descrita uma reação mediada por via imunológica. Estes pacientes apresentam obstrução das vias aéreas, com variações no PFE, sem que se demonstre significante hiper-responsividade durante a exposição ao vapor no trabalho. Níveis elevados de eosinófilos constituem-se em fator de risco para estes trabalhadores.
Poeiras — A exposição a poeiras vegetais (grãos, algodão e outras fibras têxteis) e a poeiras de animais mantidos em confinamento (estábulos etc.) podem desencadear sintomas semelhantes aos da asma, com redução nos fluxos expiratórios e aumento transitório da hiper-responsividade brônquica, associados à inflamação das vias aéreas por neutrófilos.44
Referências
01.Brooks SM. Bronchial asthma of occupational origin. Scand J Work Environ Health 1977; 3:53-72.
02.Dykewicz MS. Occupational asthma: current concepts in pathogenesis, diagnosis, and management. J Allergy Clin Immunol 2009; 123:519-30.
03.Maestrelli P, Boschetto P, Fabbri LM, Mapp CE. Mechanisms of occupational asthma. J Allergy Clin Immunol 2009; 123:531-44.
04.Mitchell CA, Gandevia B. Respiratory symptoms and skin reactivity in workers exposed to proteolytic enzymes in the detergent industry. Am Rev Respir Dis 1971; 104:1-12.
05.NIOSH Criteria for a Recommended Standard. Occupational to diisocyanates. US Dept of Health, Education and Welfare, September 1978. PHS CDC publication No. 78-215.
06.Chan-Yeung M, Ashley MJ, Corey P, Willson G, Dorken E, Grzybowski S. A respiratory survey of cedar mill workers. I. Prevalence of symptoms and pulmonary function abnormalities. J Occup Med 1978; 20:323-7.
07.Walters GI, Burge PS, Moore VC, Thomas MO, Robertson AS. Occupational asthma caused by peracetic acid-hydrogen peroxide mixture. Occup Med 2019; 69:294-297.
08.Madsen MT, Skadhauge LR, Nielsen AD, Baelum J, Sherson DL. Pyromellitic dianhydride (PMDA) may cause occupational asthma. Occup Environ Med 2019; 76:175-177.
09.Tiotiu A, Thaon I, Poussel M, et al. Occupational Asthma Caused by Powder Paint in the Automotive Industry. J Investig Allergol Clin Immunol. 2019; 29:316318.
10.Nakonechna A, Matthews D, Sargur R. Occupational asthma, rhinitis, contact dermatitis, and severe milk allergy caused by primary occupational exposure to casein. Ann Allergy Asthma Immunol 2019; 123:224225.
11.Fishwick D, Barber CM, Bradshaw LM, Harris-Roberts J, Francis M, Naylor S, Ayres J, Burge PS, Corne JM at al. Standards of care for occupational asthma. Thorax 2008: 63:240-250.
12.Barber CM, Cullinan P, Feary J, Fishwick D, Hoyle J, Mainman H, Walters GI. British Thoracic Society Clinical Statement on occupational asthma. Thorax 2022; 77:433-442.
13.Keskinen H, Alanko K, Saarinen L. Occupational asthma in Finland. Clin Allergy 1978; 8:569-79.
14.Gannon PFG, Burge PS. The SHIELD scheme in the West Midlands Redion, United Kingdom. Br J Ind Med 1993; 50:791-6.
15.Meredith S, MsDonald C. Work related respiratory disease in the United Kingdom. 1889-1992: a report of the SWORD project. Occup Med 1994; 44:183-9.
16.Baker EL. Sentinel Event Notification System for Occupational Risks (SENSOR): the concept. Am J Public Health.1989; 79 Suppl(Suppl):18-20.
17.Ameille J. Les asthmes professionnels: données épidémiologiques et résultats de l'enquête nationale. Ier Journées Thématiques: Asthme et Travail. Cité des Sciences et de l'Industrie - La Villette - Paris, 27/28 janvier 1995.
18.Work-related asthma statistics in Great Britain 2022. Disponível na internet via www. Arquivo capturado em: 07/11/2023 URL:
Work-related asthma statistics, 2022 (hse.gov.uk)
19.Baur X, Degens P, Weber K. Occupational obstructive airway diseases in Germany. Am J Ind Med 1998; 33:454-62.
20.Bernstein IL, Bernstein DI, Chan-Yeung M, Malo JL. Definition and classification of asthma. In : Bernstein IL, Chan-Yeung M, Malo J-L, Bernstein DI. Asthma in the Workplace, New York: Taylor & Francis: 2006:1-8.
21.Henneberger PK , Redlich CA , Callahan DB . Ats AD hoc Committee on Work-Exacerbated asthma. An official American thoracic Society statement: work exacerbated asthma. Am J Respir Crit Care Med 2011; 184:36878.
22.Fishwick D. Work aggravated asthma; a review of the recent evidence. Br Med Bull 2014; 110:7788.
23.Kim JL, Henneberger PK, Lohman S, Olin AC, Dahlman-Höglund A, Andersson E, Torén K, Holm M. Impact of occupational exposures on exacerbation of asthma: a population-based asthma cohort study. BMC Pulm Med 2016; 16:148.
24.Bernstein I L., Chan-Yeung, M., Malo, J.L., Bernstein, D.I. Asthma in the Workplace. New York, Marcel Dekker Inc.,1993.
25.Chan-Yeung M, Malo JL. Aetiological agents in occupational asthma. Eur Respir J 1994; 7:346-71.
26.Tarlo SM, Balmes J, Balkissoon R, Beach J, Beckett W, Bernstein D, Blanc PD, Brooks SM, Cowl CT et al.
Diagnosis and management of work-related asthma.
American College of Chest Physicians. Consensus Statement.
[published correction appears in Chest. 2008 Oct;134(4):892]. Chest 2008;134(3 Suppl):1S-41S. doi:10.1378/chest.08-0201.
27.Malo JL, Ghezzo H, D'Aquino C, L'Archeveque J, Cartier A, Chab-Yeung M. Natural history of occupational asthma: Relevance of type of agent and other factors in the rate of development of symptoms in affected subjects. J Allergy Clin Immunol 1992; 90:937-44.
28.Van Kampen V, de Blay F, Folletti I, Kobierski P, Moscato G, Olivieri M, Quirce S, Sastre J, Walusiak-Skorupa J, Raulf-Heimsoth M. EAACI position paper: skin prick testing in the diagnosis of occupational type I allergies. Allergy 2013; 68:580-584.
29.Sastre J, Fernández-Nieto M, Marañón F, Fernández-Caldas E, Pelta R, Quirce S. Allergenic cross-reactivity between nickel and chromium salts in electroplating-induced asthma. J Allergy Clin Immunol 2001; 108:650-651.
30.Quirce S, Bombín C, Alemán A, Sastre J. Allergy to latex, fruit, and pollen. Allergy 2000; 55:896-898.
31.Vandenplas O, Godet J, Hurdubaea L, Rifflart C, Suojalehto H, Wiszniewska M, Munoz X, Sastre J, Klusackova P, Moore V, Merget R, Talini D, Svanes C, Mason P, dell'Omo M, Cullinan P, Moscato G, Quirce S, Hoyle J, Sherson DL, Kauppi P, Preisser A, Meyer N, de Blay F; European network for the PHenotyping of OCcupational ASthma (E-PHOCAS) investigators. Are high- and low-molecular-weight sensitizing agents associated with different clinical phenotypes of occupational asthma? Allergy 2019; 74:261-272.
32.Brooks SM, Weiss MA, Bernstein I.L. Reactive airways dysfunction syndrome (RADS). Persistent asthma syndrome after high-level irritant exposures. Chest 1985; 88:376-384.
33.Brooks SM, Bernstein IL. Reactive airways dysfunction syndrome or irritant-induced asthma. In: Bernstein, I.L., Chang-Yeung M, Malo JL, Berstein DI, eds. Asthma in the Workplace. New York, Marcel Dekker Inc., 1993.
34.Boulet LP. Increases in airway responsiveness following acute exposure to respiratory irritants. Reactive airway dysfunction syndrome or occupational asthma? Chest 1998; 94:476-81.
35.Leroyer C, Perfetti L, Cartier A, Malo JL. Can reactive airway dysfunction syndrome (RADS) transform into occupational asthma due to sensitisation to isocyanates? Thorax 1998; 53:152-3.
36.Blanc PD, Annesi-Maesano I, Balmes JR, Cummings KJ, Fishwick D, Miedinger D, Murgia N, Naidoo RN, Reynolds CJ, Sigsgaard T, Torén K, Vinnikov D, Redlich CA. The Occupational Burden of Nonmalignant Respiratory Diseases. An Official American Thoracic Society and European Respiratory Society Statement. Am J Respir Crit Care Med 2019; 199:1312-1334.
37.Work-Related asthma in Great Britain 2020 HSE. Disponível em: https://www.hse.gov.uk statistics causdis asthma.pdfImmunology Acesso em: 10/04/2022.
38.Gibson PG, Zlatic K, Sewell W, Wolley K, Saltos N. Gene expression for GM-CSF and IL-5 in asthma and chronic cough. Am J Resp Crit Care Med 1995; 151:A779.
39.Lemière C, Efthimiadis A, Hargreave FE. Occupational eosinophilic bronchitis without asthma: an unknow occupational airway disease. J Allergy Clin Immunol 1997; 100:852-3.
40.Quirce S, Fernandez-Nieto M, de Miguel J, Sastre J. Chronic cough due to latex-induced eosinophilic bronchitis. J Allergy Clin Immunol 2001;108:143.
41.Quirce S. Eosinophilic bronchitis in the workplace. Curr Opin Allergy Clin Immunol. 2004; 4:87-91.
42.Yacoub MR, Malo JL, Labrecque M, Cartier A, Lemière C. Occupational eosinophilic bronchitis. Allergy2005; 60:1542-1544.
43.Kongerud J, Boe J, Soyseth V, Naalsund A, Magnus P. Aluminium potroom asthma: the Norwegian experience. Eur Respir J 1994; 7:165-72.
44.Merchant JA, Bernstein IL, Pickering A. Cotton and other textile dusts. In : Bernstein IL, Chang-Yeung M, Malo JL, Bernstein DI, Eds. Asthma in the Workplace . New York, Marcel Dekker, Inc., 1999; 595-616.
|
|
Home
 Design by Walter Serralheiro Design by Walter Serralheiro
|
|
|