|
Asma
TRATAMENTO DA ASMA
TEOFILINA NA ASMA
A teofilina originalmente extraída de folhas foi sintetizada em 1900. A teofilina é uma metilxantina, com estrutura similar à cafeína e à teobromina (Figura 1). Em 1930 teve sua ação broncodilatadora demonstrada em vias aéreas de porcos e em pacientes asmáticos. Há mais de 60 anos a aminofilina (sal etilenediamina da teofilina) foi introduzida por via venosa como terapêutica para as exacerbações da asma.1 Durante longo tempo foi utilizada no tratamento agudo do broncospasmo. Sua importância, entretanto, vem declinando ao longo das últimas décadas, apesar do reconhecimento recente de seus efeitos imunomoduladores e anti-inflamatórios.2
A teofilina de liberação programada tem apenas fraca eficácia na asma e os efeitos colaterais são comuns e podem ser fatais em doses mais altas. No entanto, segundo o Asthma Management and Prevention - Updated 2020 (GINA), se constitui como outra opção terapêutica nas Etapas 3-4 do manejo da asma brônquica. A teofilina continua sendo uma terapia de asma muito utilizada no mundo porque é uma droga barata, mas a grande incidência de seus efeitos colaterais e a maior eficácia das combinações de doses fixas dos corticoides inalatórios (CIs) com os broncodilatadores ß2-agonistas de longa ação (LABA) reduziram a sua utilização.
A teofilina atua inibindo as enzimas fosfodiesterases (PDEs). Esta inibição, entretanto, nas doses terapêuticas utilizadas, é fraca e não seletiva. As PDEs apresentam papel importante na regulação da atividade celular. As PDEs degradam o monofosfato cíclico de 3'5'-adenosina (AMPc) nas células inflamatórias eosinófilos, neutrófilos, macrófagos, células dendríticas, mastócitos e linfócitos T (CD4+, CD8+), assim como em células estruturais, como as epiteliais, e as células nervosas sensoriais.
O mecanismo molecular de broncodilatação da teofilina é a inibição das PDE III e PDE IV, que aumentam as concentrações intracelulares de AMPc e a inibição da PDE V que aumenta os níveis de monofosfato cíclico de 3'5'-guanosina (GMPc) na musculatura lisa brônquica e células inflamatórias.
Fosfodiesterases
Pelo menos 12 famílias geneticamente distintas de isoenzimas até agora são conhecidas. A inibição da fosfodiesterase III e IV relaxa a musculatura lisa dos brônquios e artérias pulmonares,3 enquanto que a ação imunomoduladora e anti-inflamatória resulta da inibição da isoenzima IV.4 A inibição da fosfodiesterase IV impede a ativação de mediadores da inflamação, incluindo citocinas dos eosinófilos, mastócitos, linfócitos T, macrófagos e células epiteliais. Os inibidores de PDE III não têm utilização na prática clínica devido à associação com problemas cardiovasculares, principalmente por arritmias. Na Tabela 1 apresentamos a distribuição das fosfodiesterases nas vias aéreas.
Tabela 1 - Distribuição das Fosfodiesterases nas Vias Aéreas
Tipo de Célula |
Isoforma PDE Predominante |
| Cels. Inflamatórias |
4 |
| Mastócito |
4,3 |
| Macrófago |
4 |
| Monócito |
4 |
| Eosinófilo |
4 |
| Neutrófilo |
4 |
| Plaqueta |
3,5 |
| Linfócito T |
4 |
| Cel. Endotelial |
3,4 |
| Nervo Sensorial |
4 |
| Cel. Epitelial das Vias Aéreas |
4 |
Músculo Liso |
| - vias aéreas |
3,5 |
| - dos vasos |
3,4,5 |
Pesquisas em curso são promissoras para utilização, a médio prazo, de inibidores mais potentes e seletivos da PDE tipo IV, que poderão prevenir ou reverter a hiper-responsividade brônquica e inflamação. Substâncias como rolipram, Ro 20-1724, piclamilast, tibenelast e denbufilina apresentam ação anti-inflamatória potente em modelos animais de inflamação pulmonar,5-7 porém devido aos severos efeitos colaterais não tiveram aplicação na clínica.
Inibidores seletivos de PDE IV de segunda geração, que apresentam as mesmas ações terapêuticas sem os efeitos colaterais, já estão disponíveis.8 Dentre elas o roflumilaste e o SB 207499,9 com potente ação moduladora na atividade de basófilos, monócitos, linfócitos e neutrófilos in vitro,10 suprimem o edema pulmonar e inibem também a atividade de excitação (contração) NANC, enquanto que simultaneamente potencializam a atividade de inibição (relaxamento) NANC. Bloqueiam a eosinofilia determinada por estimulação antigênica, e por ação do LTD4 em porquinhos-da-índia,11 onde se evidenciou ação broncodilatadora. Supressão de certas citocinas como IL-4 e TNF-a foi obtida em ratos.11 Apresentam também a capacidade de suprimir a mitogênese do músculo liso das vias aéreas, sugerindo que os inibidores seletivos da PDE IV possam interferir no remodelamento brônquico que ocorre na asma crônica severa.12
A maior limitação dos inibidores de PDE IV tem sido os seus efeitos colaterais, principalmente as náuseas e os vômitos. Isto ocorre provavelmente em decorrência da inibição da PDE IV no centro do vômito, que se encontra fora da barreira hemato-encefálica e cuja ação não pode ser dissociada dos efeitos anti-inflamatórios. Existem quatro isoenzimas da PDE IV humanas. A PDE IV B predomina nas células inflamatórias, enquanto que a PDE IV D parece estar mais relacionada às náuseas. O inibidor da PDE IV D mais seletivo é o cilomolaste, enquanto que o roflumilaste, não tendo esta seletividade, pode permitir que doses mais elevadas possam ser melhor toleradas. O roflumilaste apresenta propriedades anti-inflamatórias, antialérgicas, imunomodulatórias e broncodilatadoras. Mesmo o seu principal metabólito (N -óxido), em certos mamíferos de experimentação, parece também contribuir para as suas ações farmacológicas. A utilização do roflumilaste na asma encontra-se na fase III de investigação clínica.13-14
Mecanismos de Ação da Teofilina
A teofilina reduz a responsividade brônquica à histamina, aeroalérgenos, água destilada, metacolina, dióxido de enxofre e adenosina.15-17 É um potente inibidor, em concentrações terapêuticas (>10 mg.L-1) dos receptores da adenosina A1, A2A e A2B sendo menos eficaz no receptor A3.18 Embora a adenosina tenha pouca ação no músculo liso peribrônquico de normais, ela determina sua constrição em pacientes com asma, indiretamente por liberação de histamina e leucotrienos, sugerindo também liberação de outros mediadores pelos mastócitos.19 Em concentrações mais baixas (5-10 mg.L.-1), a teofilina pode ter efeitos anti-inflamatórios na asma e na DPOC, seja pela inibição de PDE IV ou, mais provavelmente, pela forte inibição da fosfoinositida-3-cinase-δ.
Outras ações da teofilina incluem a inibição de mediadores inflamatórios como as prostaglandinas, a inibição da secreção do TNF-a por monócitos do sangue periférico; o aumento da secreção da IL-10 que apresenta ação anti-inflamatória; a diminuição da fadiga muscular diafragmática e aumento de sua contratilidade;20 aumento do clearance mucociliar;21 atuação central estimulando a ventilação, o que ocorre durante a hipóxia22 e diminuição da exsudação plasmática na microcirculação brônquica.23 Embora a teofilina possa aumentar a secreção de adrenalina pela medula das suprarrenais,24 o aumento da concentração plasmática é muito pequeno para determinar efeito broncodilatador.25 Existem evidências de que a teofilina possa interferir com a mobilização do cálcio no músculo liso brônquico. A teofilina não atua na entrada dos íons cálcio (Ca2+) via canais voltagem-dependentes, entretanto, parece inibir a liberação de cálcio intracelular, atuando no turnover da fosfatidilinositol. A teofilina abre os canais de potássio Ca2+ ativados de grande condutância (KCa) da membrana plasmática do músculo liso, através da fosforilação AMPc-dependente e consequente aumento dos níveis intracelulares de AMPc. Por outro lado, a hiperpolarização da membrana associada com o relaxamento induzido pela teofilina não é essencial neste processo de broncodilatação.
A teofilina atua sobre os fatores de transcrição. Após a liberação da IkB fosforilada, o NF-kB (dímero usualmente composto por dois membros da família de proteínas Rel, o Rel A e o Rel B ) sofre translocação para o núcleo onde irá determinar a gene transcrição. A teofilina impede a degradação da proteína inibitória I-KBa, e desta forma a translocação nuclear do NF-kB (nuclear factor kB), com consequente redução da expressão de genes inflamatórios na asma.26 Estes efeitos são vistos somente a altas concentrações e podem ser mediados pela inibição da PDE.
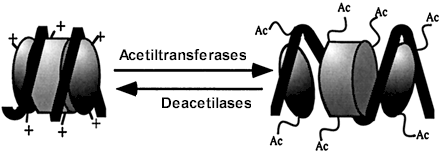 Recentemente um novo mecanismo molecular de ação anti-inflamatória da teofilina foi melhor compreendido e elucidado a ativação das histonas deacetilases (HDACs). A acetilação das histonas permite o desenrolar da estrutura local do DNA, remodelando a cromatina, liberando o acesso para a ação de fatores de transcrição. A acetilação é regulada por um balanço entre a atividade das acetiltransferases das histonas (HATs) e das histonas deacetiltransferases (HDACs) (Figura 2). Recentemente um novo mecanismo molecular de ação anti-inflamatória da teofilina foi melhor compreendido e elucidado a ativação das histonas deacetilases (HDACs). A acetilação das histonas permite o desenrolar da estrutura local do DNA, remodelando a cromatina, liberando o acesso para a ação de fatores de transcrição. A acetilação é regulada por um balanço entre a atividade das acetiltransferases das histonas (HATs) e das histonas deacetiltransferases (HDACs) (Figura 2).
Alterações na atividade HAT e HDAC podem atuar em doenças inflamatórias crônicas. Em estudos recentes, fragmentos de biópsias brônquicas de pacientes com asma evidenciam expressão de altos níveis de atividade HAT e baixa atividade HDAC, sugerindo que um desequilíbrio HAT-HDAC possa ser o substrato para a gene expressão pró-inflamatória. Pacientes com asma têm níveis basais reduzidos de HDAC. Embora os corticoides aumentem os níveis de HDAC em pacientes com asma, estes níveis permanecem bem abaixo daqueles induzidos pelos corticoides em indivíduos normais.27 Este fato sugere que substâncias que aumentem a atividade HDAC, como a teofilina, mesmo em baixas doses, propiciam atividade aditiva terapêutica sobre a ação dos esteroides, reduzindo a gene transcrição inflamatória.28
A teofilina ativa diretamente as HDACs, as quais deacetilam o núcleo das histonas que foram acetilados pela atividade de coativadores como a cAMP response element binding protein (CREB)- binding protein (CBP). Isto resulta em supressão de genes inflamatórios e proteínas, que seriam ativados por fatores de transcrição pró-inflamatórios como o NF-kB e a AP-1 (activator protein-1), pois ocorre uma redução na acetilação da histona e restauração da estrutura densa da cromatina, o que inibe a ligação de fatores de transcrição (Figura 3).
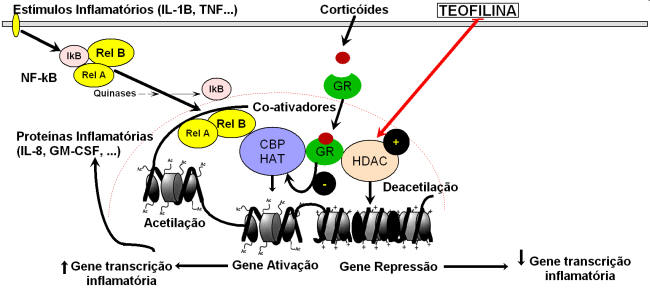
A ação da teofilina aumentando a atividade da HDAC ocorre em doses terapêuticas de 10-6 – 10-5 M, sendo praticamente nula a concentrações maiores (10-4 M). Esta propriedade terapêutica pode ser bloqueada pela tricostatina A, substância que inibe a HDAC. Um significante aumento na atividade HDAC é encontrado em biópsias brônquicas após tratamento de pacientes com asma com baixas doses de teofilina (concentrações plasmáticas médias ~5 mg/L). A teofilina ativa preferencialmente as HDACs da classe I, incluindo a HDAC2, de grande importância na redução da gene transcrição inflamatória.
Os corticoides também ativam as HDACs, só que por um mecanismo diferente, resultando no recrutamento das HDACs para o complexo transcricional ativado, via ativação de receptor de corticoide (GR), que atua como molécula ponte. É muito provável que corticoides e teofilina possam juntos reprimir a expressão gene inflamatória de forma sinérgica.
Estudos recentes sugerem que a teofilina atue aumentando a atividade da HDAC, que é recrutada pelos corticoides ao complexo de transcrição, a fim de inibir os genes inflamatórios, aumentando a eficácia dos corticoides.27 O mecanismo pelo qual baixas doses de teofilina ativam a HDAC ainda não é conhecido. Entretanto, sabe-se não ser mediado pela inibição de PDE ou por antagonismo do receptor de adenosina, porque inibidores PDE (não seletivo, inibidores PDE III e PDE IV) e antagonistas de receptores de adenosina A1 e A2 não mimetizam esta ação da teofilina. As HDACs não são efetivas na inativação de genes inflamatórios a menos que recrutadas para o sítio ativo inflamatório, por receptores de corticoide ativados. A ação anti-inflamatória da teofilina quando de seu uso isolado é considerada fraca. Quando associada ao corticoide, a teofilina mesmo em doses baixas potencializa os efeitos dos corticoides in vitro, em cerca de 100 a 1.000 vezes.28 Várias publicações confirmam estes dados, quando foram avaliadas associações de baixas doses de teofilina com baixas e altas doses de esteroides.29-31
As atuais diretrizes internacionais não recomendam o uso da teofilina no tratamento da asma porque um CI é muito mais eficaz quando combinado com um LABA do que com teofilina de liberação sustentada.32 No enanto, a teofilina pode induzir broncodilatação adicional, mesmo quando da administração de doses máximas eficazes de um ß2-agonista.33 Assim, os dois
podem ser combinados de maneira útil em algumas circunstâncias específicas. Além disso, a teofilina pode ajudar no tratamento da asma noturna devido a preparações de liberação programada e garantir a manutenção das concentrações terapêuticas durante a noite, embora sejam menos eficazes do que um LABA. Uma série de estudos demonstrou que a teofilina provoca efeitos que propiciam a redução das doses de corticoides.34,35
Baseados nos conhecimentos modernos dos mecanismos moleculares da ação anti-inflamatória da teofilina, vários estudos preconizam a sua associação com corticoides por inalação, mesmo em doses subterapêuticas (5-10 mg/l).36 Acreditam que esta associação implique sinergismo, potencializando os efeitos anti-inflamatórios dos corticoides, com menos efeitos colaterais.2,37 Em certos pacientes, ao invés de se aumentar a dose de corticoide por inalação, a associação com a teofilina, pode resultar em maior efeito supressivo da expressão de genes inflamatórios.
Os efeitos colaterais mais comuns são a cefaleia, náuseas, vômitos (por inibição da PDE IV no centro do vômito),38 dor abdominal, irritabilidade, diarreia e tremores. A estimulação do SNC, arritmias cardíacas (através da desacetilação do receptor adeno-A1) quando de concentração plasmática >20 mg/l, hipersecreção gástrica (inibição da PDE IV nas glândulas parietais), refluxo gastresofágico e aumento da diurese ocorrem devido ao antagonismo ao receptor da adenosina.37 Convulsões ocorrem quando de altas concentrações plasmáticas (>30 mg/l) em pacientes com asma grave e quando a via de administração é venosa.
A teofilina é rápida e completamente absorvida pelo trato gastrintestinal. É metabolizada no fígado pelo sistema enzimático microssomal citocromo P-450/P-448, principalmente pela enzima CYP1A2 (cytochrome P450, family 1, subfamily a, polypeptide 2), com participação da CYP2E1 (cytochrome P450, family 2, subfamily E, polypeptide 1) quando de altas concentrações plasmáticas.40 Drogas que inibem a CYP1A2, como macrolídeos, quinolonas, podem elevar os níveis plasmáticos da droga e determinar toxicidade.
O clearance da teofilina está aumentado em 60-100% em fumantes quando comparado a não-fumantes, resultando em um declínio de quase duas vezes na meia-vida da droga, quando comparado a de não-fumantes. A exposição crônica ambiental à fumaça do cigarro aumenta o clearance da teofilina,41 porém este efeito não é encontrado imediatamente após a aguda exposição ambiental.42 Crianças com asma, crônicamente expostas à fumaça de cigarro, têm um aumento de 51% no clearance da teofilina e redução de 24% nos níveis séricos quando se compara aos de crianças em espaços sem exposição à fumaça do cigarro.43 Na Tabela 2 são descritos outros fatores que interferem no clearance da teofilina.
Tabela 2 – Fatores que Interferem no Clearance da Teofilina
Aumentam o Clearance |
| Indução enzimática (rifampicina, etanol) |
| Tabagismo |
| Dietas ricas em proteínas e pobres em carboidratos |
| Crianças |
Diminuem o Clearance |
| Inibição enzimática (quinolonas, macrolídeos, alopurinol, ...) |
| Hepatopatia |
| Pneumonia |
| Vacinação e infecção viral |
| Dieta rica em carboidrato |
| Senilidade |
Doxofilina
Doxofilina [7- (1,3-dioxolan-2-ilmetil) -3,7-di-hidro-l, 3 dimetilH-purina-2,6-diona] é uma metilxantina de nova geração com atividade tanto broncodilatadora como anti-inflamatória. A presença do grupo dioxolano na posição 7 a torna com um novo perfil que não deve ser considerada como uma teofilina modificada.44
Está indicada para o tratamento da doença pulmonar obstrutiva crônica (DPOC), asma e doenças pulmonares com componente espástico. Como droga usada no tratamento da asma, a doxofilina demonstrou eficácia semelhante à teofilina, porém com menos efeitos adversos em estudos com animais e humanos. Apresenta baixa afinidade pelos receptores alfa-1 ou alfa-2 da adenosina e não apresenta efeitos estimulantes. A doxofilina não interage com qualquer uma das isoformas de PDE conhecidas, exceto para PDE2A1 e sua ação farmacológica não é influenciada por qualquer uma das enzimas histona desacetilases conhecidas.45 Interage, entretanto, com os receptores ß2-agonistas do músculo liso vascular e das vias aéreas provocando relaxamento.46 Ao contrário da teofilina, a doxofilina não afeta o influxo de cálcio e não antagoniza as ações dos bloqueadores dos canais de cálcio, o que poderia explicar a redução das reações adversas cardíacas associadas ao medicamento.47 Uma diferença farmacocinética primordial entre a doxofilina e a teofilina reside no fato de que a doxofilina não interfere com as enzimas CYP1A2, CYP2E1 e CYP3A4 do citocromo P450, o que permite não interagir com outras drogas metabolizadas por meio dessas vias no fígado.48 A doxofilina leva a uma redução na necessidade de corticoide, embora as xantinas também tenham uma janela terapêutica estreita que limita seu uso mais amplo. Esse efeito poupador de corticoide pôde ser demonstrado em um estudo com modelo de inflamação pulmonar tanto em murídeos alérgicos como não alérgicos quando resultados sugeriram que a droga apresenta efeitos anti-inflamatórios significativos.49
Em pacientes com asma, a doxofilina não foi significativamente diferente da teofilina no aumento do VEF1, na redução da ocorrência de episódios de asma, ou no uso de salbutamol como medicamento para aliviar os sintomas agudos.50 No entanto, a doxofilina é uma metilxantina eficaz e segura para o tratamento da asma, com um perfil de eficácia / segurança superior ao da teofilina.51
Roflumilaste
Roflumilaste é um inibidor PDE-IV utilizado por via oral, que determina inibição do broncospasmo da fase tardia da asma, após provocação alergênica em pacientes com asma leve. Utilizando-se a dose máxima de 500 mcg, o roflumilaste reduziu a resposta tardia em 43% vs placebo (p = 0,0009).52 A resposta na fase precoce da doença também foi reduzida porém, em menor intensidade - 28% (p = 0,0046). Em um estudo subsequente,53 a terapia com roflumilaste na dose de 500 mcg em dose única diária determinou melhora similar na função pulmonar e nos sintomas da asma persistente, com redução na medicação de resgate, v. terapia com beclometasona, na dose de 200 mcg duas vezes ao dia. Em um estudo randomizado, duplo-cego, em grupos paralelos, estudo fase 2/3,54 os pacientes receberam roflumilaste por 12 semanas. Doses de 100, 250 e 500 mcg aumentaram significativamente o VEF1 (p< 0,001 v. basal) com aumentos a partir do basal na última visita de 400 ml para o grupo que utilizou a dose máxima (500 mcg) v. o grupo com a menor dose (100 mcg). Ocorreu ainda melhora significante a partir dos parâmetros basais matinais e vespertinos do PFE para todas as doses (p< 0,006).
Uma outra droga que inibe a PDE-IV encontra-se em fase de investigação, o ciclamilaste. Estudos em modelos de ratos sugerem que este agente medeia a hiper-responsividade brônquica através da inibição da expressão do RNA mensageiro PDE-IV D e determina a downmodulation da atividade PDE-IV, com redução da inflamação e da hipersecreção de muco.55.
Referências
01.Segal MS, Levinson L, Bresnik E. Evaluation of therapeutic substances employed for the relief of bronchospasm. VI. Aminophilline. J Clin Invest 1949; 28:1190-5.
02.Weinberger M, Hendeles L. Theophylline in asthma. N Engl J Med 1996; 334:1380-8.
03.Rabe KF, Tenor H, Dent G, Nakashima M, Schudt C, Magnussen H. Theophylline relaxes human airways and pulmonary arteries in vitro through phosphodiesterase inhibition. Am Rev Respir Dis 1993; 147(suppl):A184, abstract.
04.Lagente V, Pruniaux MP, Junien JL, Moodley I. Modulation of cytokine-induced eosinophil infiltration by phosphodiesterase inhibitors. Am J Respir Crit Care Med 1995; 151:1720-4.
05.Torphy TJ, Undem BJ. Phosphodiesterase inhibitors:new opportunities for the treatment of asthma. Thorax 1991; 46:512-23.
06.Torphy TJ. Phosphodiesterase isozymes: molecular targets for novel antiasthma agents. Am Respir Crit Care Med 1998; 157:351-70.
07.Giembycz MA, Dent G. Prospects for selective cyclic nucleotide phosphodiesterase inhibitors in the treatment of bronchial asthma. Clin Exp Allergy 1992; 22:337-44.
08.Compton CH, Cedar E, Nieman RB, Amit O, Langley SJ, Sapene M. Ariflo TM improves pulmonary function in patients with asthma: Results of a study in patients taking inhaled corticosteroids. Am J Crit Care Med 1999; 159:A522.
09.Torphy TJ, Barnette DC, Underwood DC, Griswold DE, Christensen SB. Ariflo TM (SB 207499), a second generation phosphodiesterase 4 inhibitor for treatment of asthma and copd: from concept to clinic. Pulmonary Phermacology & Therapeutics 1999; 12:131-5.
10.Barnette MS, Christensen SB, Essayan DM, Grous M, Prabhakar U, Rush JA, Kagey-Sobotks A, Torphy TJ. SB 207499 (Ariflo TM ), a potent and selective second-generation phosphodiesterase 4 inhibitor: in vitro antiinflammatory actions. J Pharmacol Exp Ther 1998; 284:420-6.
11.Underwood DC, Bochnowicz S, Osborn RR, Kotzer CJ, Luttman MA, Hay DWP, Gorycki PD, Christensen SB,Torphy TJ. Anti-asthmatic activity of the second generation phosphodiesterase 4 inhibitor, SB 207499 (Ariflo TM ), in the guinea pig. J Pharmacol Exp Ther 1998; 287:988-95.
12.Panettieri RA, Eszterhas A, Cieslinski LB, Torphy TJ. Ariflo ® (SB 207 499) modulates human airway smooth muscle cell proliferation induced by mit o gens. AM J Respir Crit Care Med 2000; 161:A697.
13.Hatzelmann A, Schudt C. Anti-inflammatory and immunomodulatory potential of the novel PDE4 onhibitor roflumilast in vitro. JPET 2001; 297:267-79.
14.Bundschuh DS, Eltze M, Barsig J, Wollin B, Hatzelmnn A, Beume R. In vivo efficacy in airway disease models of roflumilast, a novel orally active PDE4 inhibitor. JPET 2001; 297:280-90.
15.Magnussen H, Reuss G, Jorres R. Theophylline has a dose-related effect on the airway response to inhaled histamine and methacholine in asthmatics. Am Rev Respir Dis 1987; 136:1163-7.
16.Koenig JQ, Dumler K, Rebolleledo V, Williams PV, Pierson WE. Theophylline mitigates the bronchoconstrictor effects of sulfur dioxide in subjects with asthma. J Allergy Clin Immunol 1992; 86:789-94.
17.Holgate ST, Mann JS, Cushley MJ, Adenosine as a broncoconstritor mediator in asthma and its antagonism by metilxanthines. J Allergy Clin Immunol 1984; 74:302-06.
18.Pauwels RA, Joos GF. Characterization of the adenosine receptors in airways. Arch Int Pharmacodyn Ther 1995; 329:151-60.
19.Björk T, Gustafsson LE, Dahlén S. Isolated bronchi from asthmatics are hiperresponsive to adenosine, which apparently acts indirectly by liberation of leukotrienes and histamine. Am Rev Respir Dis 1992; 145:1087-91.
20.Murciano D, Aubier M, Lecocguic Y, Pariente R. Effects of theophylline on diaphragmatic strength and fatigue in patients with chronic obstructive pulmonary disease. N Engl J Med 1984; 311:349-53.
21.Cotromanes E, Gerrity TR, Garrard CS, et al. Aerosol penetration and mucociliary transport in healthy human lung: effect of low serum theophylline levels. Chest 1985; 88:194-200.
22.Easton PA, Anthonisen NR. Ventilatory response to sustained hypoxia after pretreatment with aminophylline. J Appl Physiol 1988; 64:1445-50.
23.Erjefalt I, Persson CG. Anti-asthma drugs attenuate inflammatory leakage of plasma into airway lumen. Acta Physiol Scand 1986; 128:653-4.
24.Ishizaki T, Minegishi A, Morishita A et al. Plasma catecholamine concentrations during a 72 hour aminophylline infusion in children with acute asthma. J Allergy Clin Immunol 1988; 92:146-54.
25.Barnes PJ. Endogenous catecholamines and asthma. J Allergy Clin Immunol 1986; 77:791-5.
26.Tomita K, Chikumi H, Tokuyasu H et al. Functional assay of NF-KappaB translocation into nuclei by laser scanning cytometry: inhibitory effect by dexamethasone or theophylline. Naunyn Schmiedebergs Arch Pharmacol 1999; 359:249-55.
27.Ito K, Lim S, Adcock IM, Caramori G, Keller A, Barnes PJ. Effect of low dose theophylline on histone deacetylase activity in patients with mild asthma. Am J Resp Crit Care Med 2000; 161:A614.
28.Ito K, Lim S, Caramori G, Cosio B, Chung KF, Ad cock IM, Barnes PJ. A molecular mechanism of action of theophylline: induction of histone deacetylase activity to decrease inflammatory gene expression. Proc Natl Acad Sci USA 2002; 99:8921-6.
29.Evans DJ, Taylor DA, Zetterstrom O, Chung KF, O'Connor BJ, Barnes PJ. A comparison of low-dose inhaled budesonide plus theophylline and high-dose inhaled budesonide for moderate asthma. N Engl J Med 1997; 337:1412-8.
30.Ukena D, Harnest U, Sakalauskas R, Magyar P, Vetter N, Steffen H, Leichtl S, Rathgeb F, Keller A, Steinijans VW. Comparison of addition of theophylline to inhaled steroid with doubling of the dose of inhaled steroid in asthma. Eur Respir J 1997; 10:2754-60.
31.Lim S, Tomita K, Carramori G, Jatakanon A, Oliver B, Keller A, Adcock I, Chung KF, Barnes PJ. Low-dose theophylline reduces eosinophilic inflammation but not exhaled nitric oxide in mild asthma. Am J Respir Crit Care Med 2001; 164:273.
32.Adachi M, Aizawa H, Ishihara K, Ohta K, Sano Y, Taniguchi H, Nakashima M. Comparison of salmeterol/fluticasone propionate (FP) combination with FP1 sustained release theophylline in moderate asthma patients. Respir Med 2008; 102:1055-1064.
33.Bonini M, Usmani OS. Drugs for airway disease. Medicine (Baltomore) 2016; 44:271-280.
34.Markham A, Faulds D. Theophylline. A review of its potential steroid sparing effects in asthma. Drugs 1998; 56:1081-1091.
35.Spina D, Page CP. Xanthines and Phosphodiesterase inhibitors. Handb Exp Pharmacol 2017; 237:63-91.
36.Barnes PJ, Pauwels RA. Theophylline in asthma: time for reappraisal? Eur Respir J 1994; 7:579-91.
37.Kidney J, Dominguez M, Taylor PM, Rose M, Chung KF, Barnes PJ. Immunomodulation by theophylline in asthma. Am J Respir Crit Care.Med 1995; 151:1907-14.
38.Nicholson CD, Challiss RAJ, Shahid M. Differential modulation of tissue function and therapeutic potential of selective inhibitors of cyclic nucleotide phosphodiesterase is enzymes. Trends Pharmacol Sic 1991; 12:19-27.
39.Barnes JB, Rodger IW, Thomson NC. Asthma - Basic Mechanisms and Clinical Management . London, Academic Press, 3rd ed., 1998 .
40.Zhang ZY, Kaminsky LS. Characteization of human cytochromes P450 involved in theophylline 8-hydroxylation. Biochemical Pharmacol 1995; 50:205-11.
41.Matsunga SK, Plezia PM, Karol MD, Katz MD, Camilli AE, Benowitz NL.
Effects of passive smoking on theophylline clearance. Clin Pharmacol Ther 1989; 46:399-407.
42.Castro D, Schnapf B, Clotz M. Lack of effect of short-term passive smoking on the metabolic disposition of theophylline. Eur J Clin Pharmacol 1990; 39:399-402.
43.Mayo P. Effect of passive smoking on theophylline clearance in children. Ther Drug Monit 2001; 23:503-5.
44.Matera MG, Page C, Cazzola M. Doxofylline is not just another theophylline!. Int J Chron Obstruct Pulmon Dis 2017; 12:3487-3493.
45.van Mastbergen J, Jolas T, Allegra L, Page CP. The mechanism of action of doxofylline is unrelated to HDAC inhibition, PDE inhibition or adenosine receptor antagonism. Pulm Pharmacol Ther 2012; 25:55-61.
46.Zhang Y, Zeng K, Wang J, Gao H, Nan Y, Zheng X. Identifying the antiasthmatic target of doxofylline using immobilized b2-adrenoceptor based highperformance affinity chromatography and site-directed molecular docking. J Mol Recognit 2016; 29:492-498.
47.Shukla D, Chakraborty S, Singh S, Mishra B: Doxofylline: a promising methylxanthine derivative for the treatment of asthma and chronic obstructive pulmonary disease. Expert Opin Pharmacother 2009; 10:2343-56.
48.Lazzaroni M, Grossi E, Bianhi Porro G. The effect of intravenous doxofylline or aminophylline pn gastric secretion in duodenal ulcer patients. Aliment Pharmacol Ther 1990; 4:643-649.
49.Riffo-Vasquez Y, Venkatasamy R, Page CP. Steroid sparing effects of doxofylline. Pulm Pharmacol Ther 2018; 48:1-4.
50.Calzetta L, Hanania NA, Dini FL, Goldstein MF, Fairweather WR, Howard WW, Cazzola M. Impact of doxofylline compared to theophylline in asthma: a pooled analysis of functional and clinical outcomes from two multicentre, doubleblind, randomized studies (DOROTHEO 1 and DOROTHEO 2). Pulm Pharmacol Ther 2018; 53:20-26.
51.Rogliani P, Calzetta L, Ora J, Cazzola M, Matera MG. Efficacy and safety profile of doxofylline compared to theophylline in asthma: a meta-analysis. Multidiscip Respir Med 2019; 14:25.
52.van Schalkwyk E, Strydom K, Williams Z et al. Roflumilast, an oral, once-day phosphodiesterase 4 inhibitor, attenuates allergen-induced asthmatic reactions. J Allergy Clin Immunol 2005; 116:292-298.
53.Bousquet J, Aubier M, Sastre J et al. Comparison of roflumilast, an oral anti-inflammatory, with beclomethasonedipropionate in the treatment of persistent asthma. Allergy 2006; 61:72-78.
54.
Bateman ED, Izquierdo JL, Harnest U, Hofbauer P, Magyar P, Schmid-Wirlitsch C, Leichtl S, Bredenbröker D. Efficacy and safety of roflumilast in the treatment of asthma. Ann Allergy Asthma Immunol 2006; 96:679-686.
55.Deng YM, Xie QM, Tang HF et al. Effects of ciclamilast, a new PDE e PDE4 inhibitor, on airway hyperresponsiveness, PDE4D expression and airway inflammation in a murine model of asthma. Eur J Pharmacol 2006; 547:125-135.
|
|
Home
 Design by Walter Serralheiro Design by Walter Serralheiro
|
|
|