A rinite alérgica (RA) é classificada como sazonal ou perene conforme o período e a duração da exposição ao alérgeno, fatores que também influenciam sua patogênese. Normalmente, cerca de 20% dos casos são exclusivamente sazonais, 40% perenes e os outros 40% apresentam um padrão misto, definido por sintomas contínuos com piora em determinadas épocas do ano.1
A RA afeta de 10 a 40% da população mundial.2 "De acordo com o Global Asthma Report 2022 , a prevalência de sintomas de RA em adolescentes em centros urbanos selecionados já ultrapassa 30%, refletindo os dados da Fase I da Global Asthma Network (GAN)."3 No Brasil, os estudos de centros específicos como a cidade de Uruguaiana (RGS), publicados em 2023 mostram que a média de diagnóstico médico de rinite em adultos já está em 31,7% e em adolescentes em 28,0%.4
Embora a rinite não seja uma condição que ameace a vida, ela pode afetar significativamente a qualidade de vida e ser responsável pela perda de produtividade nos estudos e no trabalho. Os pacientes apresentam como queixas prurido nasal, congestão, rinorreia, tosse e espirros. Outas manifestações incluem o gotejamento pós-nasal, o lacrimejamento, o prurido no palato e nos ouvidos, além de ser acompanhada por sintomas oculares (conjuntivite).5
A RA perene caracteriza-se pela inflamação crônica da mucosa nasal, resultante de reação de hipersensibilidade a alérgenos presentes de forma contínua no ambiente do paciente ao longo de todo o ano. Os principais desencadeantes incluem pólen, alérgenos domiciliares (como ácaros da poeira, pelos e escamas de animais domésticos) e, em alguns casos, alérgenos ocupacionais.5
A rinite alérgica está frequentemente associada à asma. Estima-se que 10% a 40% dos pacientes com RA apresentam asma,6 enquanto sintomas nasais estão presentee em 6 a 85% dos pacientes asmáticos.7-10 A RA é considerada um fator de risco para o desenvolvimento da asma,10 e a forma moderada a grave não controlada pode prejudicar o controle da doeça.11,12 Ambas compartilham os mesmos gatilhos, mediadores inflamatórios e mecanismos imunológicos.
Em 1997 Grossman argumentava que a asma e a rinite não deviam ser vistas como doenças dissociadas, porém como manifestações de um mesmo processo inflamatório nas vias aéreas. Nesse artigo já salientava que 60–78% dos pacientes com asma apresentavam RA. Surgiu assim o conceito de "Via Aérea Única" ou "One Airway, One Desease", pois as vias aéreas superiores e inferiores constituem uma unidade anatômica e imunológica, onde os processos inflamatórios se manifestam como um continuum.13
Em 2001 foi publicado pela primeira vez o estudo Allergic Rhinitis and its Impact on Asthma (ARIA),14 com constantes atualizações desde então. Essa diretriz introduziu a classificação de rinite intermitente vs. persistente e leve vs. moderada-grave substituindo, a antiga classificação sazonal/perene. Na primeira grande revisão ARIA em 2008 baseada em evidências ocorreu a consolidação da relação rinite-asma como doença única das vias aéreas.15 Em 2016 despontou o conceito de real-world evidence e a utilização do aplicativo MASK-rhinitis para monitoramento de sintomas, destacando-se a necessidade de mais pesquisa.16 Em 2019 surgiu a aplicação formal da metodologia GRADE (Grading of Recommendating Assessment, Development and Evaluation). Em 2023 ocorreu o uso mais estruturado da sistematização GRADE, com integração do real-world evidence com ensaios clínicos e maior foco em tratamento individualizado à medicina de precisão.17
Um ponto conceitual interessante nesses estudos mostra que tratar rinite com corticoide intranasal (CIN) não substitui o uso do corticoide inalado (CI) na asma, no entanto, melhora o controle global da doença das vias aéreas.
A relação de agravamento entre rinite crônica e asma possui uma fundamentação fisiopatológica robusta, reforçando o conceito de doença única das vias aéreas. O conceito se baseia na interação que ocorre através de mecanismos anatômicos, imunológicos, neurogênicos e inflamatórios. Hoje é consenso que a rinite é muito comum em asmáticos, piora a qualidade de vida destes pacientes e a percepção de controle da doença, sendo que tratar a rinite é mandatório, mas não exclui o tratamento adequado da asma.
O nariz é revestido por três tipos diferentes de epitélio:
● epitélio escamoso estratificado, presente no vestíbulo nasal e nasofaringe;
● epitélio colunar pseudoestratificado ciliado, que recobre a maior parte da cavidade nasal respiratória;
● epitélio olfativo especializado, com células receptoras ciliadas na área olfatória superior.
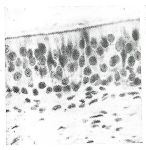 A porção anterior do nariz forma o vestíbulo nasal, revestido por pele semelhante à da face, como se houvesse uma invaginação cutânea. Nessa região há pelos curtos e rígidos altamente sensíveis a estímulos mecânicos capazes de desencadear prurido e espirros, que não respondem à simples passagem de ar durante a respiração. O epitélio escamoso estratificado do vestíbulo possui características sensoriais semelhantes às da pele facial, incluindo termorreceptores que detectam o resfriamento do ar inspirado. A porção restante é semelhante à das vias aéreas inferiores, do tipo pseusoestratificado e ciliado com células basais, caliciformes e colunares ciliadas e não ciliadas; com infiltrado celular inflamatório similar – mastócitos, neutrófilos, basófilos, eosinófilos, linfócitos Th2 – e expressão semelhante de mediadores. A camada epitelial repousa sobre um substrato de tecido conjuntivo, consistindo de membrana basal, uma camada de tecido conjuntivo composta de colágenos tipo III, IV e V, laminina e fibronectina. A lâmina própria apresenta a característica de ser altamente vascularizada. Desta forma, a inflamação de uma parte do sistema respiratório pode se propagar funcionalmente para outra.18
A porção anterior do nariz forma o vestíbulo nasal, revestido por pele semelhante à da face, como se houvesse uma invaginação cutânea. Nessa região há pelos curtos e rígidos altamente sensíveis a estímulos mecânicos capazes de desencadear prurido e espirros, que não respondem à simples passagem de ar durante a respiração. O epitélio escamoso estratificado do vestíbulo possui características sensoriais semelhantes às da pele facial, incluindo termorreceptores que detectam o resfriamento do ar inspirado. A porção restante é semelhante à das vias aéreas inferiores, do tipo pseusoestratificado e ciliado com células basais, caliciformes e colunares ciliadas e não ciliadas; com infiltrado celular inflamatório similar – mastócitos, neutrófilos, basófilos, eosinófilos, linfócitos Th2 – e expressão semelhante de mediadores. A camada epitelial repousa sobre um substrato de tecido conjuntivo, consistindo de membrana basal, uma camada de tecido conjuntivo composta de colágenos tipo III, IV e V, laminina e fibronectina. A lâmina própria apresenta a característica de ser altamente vascularizada. Desta forma, a inflamação de uma parte do sistema respiratório pode se propagar funcionalmente para outra.18
A RA ocorre quando o sistema imunológico se sensibiliza a um ou mais alérgenos ambientais. Durante esse processo, o organismo passa a produzir anticorpos IgE específicos, que se fixam a receptores de alta afinidade (FcεRI) pesentes na superfície de mastócitos e basófilos. Essa tendência de certos organismos em desenvolver respostas imunes mediadas por IgE é herdada por pacientes atópicos. Quando o indivíduo é novamente exposto ao alérgeno, ocorre a ligação cruzada dessas IgEs, pois um número crescente de mastócitos revestidos por IgE atravessa o epitélio, reconhece o alérgeno depositado na mucosa e sofre desgranulação, desencadeando a liberação de mediadores inflamatórios como histamina, prostaglandinas e leucotrienos. Essa fase é conhecida como fase imediata da reação alérgica, responsável por sintomas como prurido nasal, espirros, congestão e rinorreia.1,5
Na fase tardia, que contribui para a manutenção e cronificação do quadro, citocinas e quimiocinas liberadas localmente promovem o recrutamento de linfócitos Th2, eosinófilos e basófilos. Essas células intensificam a resposta inflamatória ao liberar mediadores como IL-4, IL-5 e IL-13, agravando a inflamação da mucosa nasal, perpetuando os sintomas.
Diversos mecanismos têm sido propostos para a interação entre as vias aéreas superiores e inferiores na rinite alérgica e na asma.19 Acredita-se que ocorra uma conexão com migração de células inflamatórias, particularmente os eosinófilos, entre vias aéreas superiores e os brônquios, por via sistêmica, através da corrente sanguínea e pela participação da medula óssea ativada, liberando mediadores na circulação que se deslocam até a mucosa. Em consequência ocorre aumento da hiper-responsividade brônquica (HRB) e da inflamação das pequenas vias aéreas, amplificando-a. A rinite crônica contribui para a gravidade da asma porque "propaga" a inflamação da mucosa nasal local por via sistêmica para as vias aéreas inferiores.
O sintoma nasal é apenas o indício de que a inflamação eosinofílica muitas vezes já está presente nas vias aéreas inferiores.20
O reflexo naso-brônquico ocorre através de mecanismo fundamentado na inervação da mucosa nasal por fibras aferentes (trigeminais e olfatórias ) e eferentes (simpáticas e parassimpáticas). A inflamação nasal ativa receptores trigeminais, cujas fibras terminais – distribuídas em glândulas submucosas, epitélio, tecido conjuntivo e vasos – desencadeiam reflexos neurogênicos, como espirros, hipersecreção, ou a própria inflamação neurogênica.18
O sistema NANC constitui o terceiro sistema nervoso autônomo. Esses neurônios liberam neuropeptídeos como a substância P (SP), o peptídeo relacionado ao gene da calcitonina (CGRP), a neurocinina A (NKA) e o peptídeo liberador de gastrina (GRP). Tais mediadores são responsáveis pelas sensações de prurido, pressão, além de induzirem a contração do músculo liso peribrônquico e a hipersecreção das glândulas submucosas. Em suma, a interação rinite-asma pelo reflexo naso-brônquico é essencialmente mediada por nervos sensoriais e pela ação desses neuropeptídeos.21
Estudos experimentais utilizando teste de provocação nasal obtiveram aumento em marcadores de inflamação alérgica nas vias aéreas inferiores,22 indução na HRB por meio da liberação de SP pelos nervos pulmonares.21.23
Perda da Função Fisiológica
O nariz é a porta de entrada do sistema respiratório, sendo três as funções quando da passagem do ar: 1) o ar é aquecido em contato com a ampla superfície dos cornetos e do septo; 2) o ar é umidificado quase que completamente antes de deixar o nariz; 3) filtração de partículas.
Na rinite crônica a inflamação e congestão da mucosa prejudicam sua função de filtrar partículas como alérgenos e poluentes. Quando de obstrução nasal, ocorre respiração oral e em consequência entrada de ar mais frio e mais seco com partículas diretamente aos brônquios que são mais reativos em um asmático. Isso aumenta a hiper-responsividade e leva à maior inflamação das vias aéreas.
Tratamento
O painel ARIA contribui para aperfeiçoar o manejo da rinite alérgica, utilizando metodologia GRADE ao mesmo tempo que incorpora evidências do mundo real. É um guia farmacoterapêutico da rinite. Este consenso enfatiza estratégias terapêuticas, comparando classes terapêuticas, adesão ao tratamento e utiliza algorítimos digitais. Com a utilização do MASK-Air, desenvolvido pelo ARIA, este aplicativo móvel voltado para o monitoramento de sintomas de rinite e asma, aportou algumas informações interessantes como, p. ex., a constatação de dados demonstrando que os pacientes preferem muito mais os anti-histamínicos, mesmo sendo menos eficazes do que os corticoides intranasais (CINs)24,25— algo que ajuda a explicar o motivo pelo qual a rinite permanece subtratada no âmbito global.
Os resultados combinados de dois estudos com mais de 9.000 usuários em 22 países25,26 apontam que na vida real são verdadeiras as seguintes afirmações: (i) os pacientes apresentam baixa adesão ao tratamento, e a maioria se automedica. (ii) A maioria dos pacientes com RA utiliza o tratamento conforme a necessidade, quando mal controlados.23 (iii) A grande maioria não segue as diretrizes ou prescrições médicas.24-26
Conceitualmente, é fundamental destacar que, sem o tratamento adequado da rinite, torna-se difícil controlar a asma. No entanto, tratar apenas a rinite não substitui o manejo específico da asma. É essencial orientar os pacientes sobre a importância de manter adesão ao tratamento mesmo durante períodos assintomáticos, realizando qualquer ajuste terapêutico somente sob supervisão médica, evitando deste modo a automedicação.
Os alérgenos presentes no ambiente domiciliar são reconhecidos como importantes desencadeadores de sintomas tanto de rinite quanto de asma. Assim, o controle da exposição a esses alérgenos constitui parte relevante do tratamento das doenças alérgicas. Saber o que causa pode ajudar a evitar os fatores desencadeantes. Apesar disso, ainda são necessárias mais pesquisas sobre estratégias e métodos de persuasão que favoreçam a adesão dos pacientes a essas medidas ambientais.
É recomendado tratar tanto a RA como a asma, de acordo com as Diretrizes da GINA, pois o não tratamento acarreta mais visitas às emergências, mais internações e pior qualidade no sono.27 Estudos demonstram que o uso de CINs está associado a Risco Relativo de aproximadamente ≈ 0,7 em comparação a não usuários, evidenciando um efeito protetor. Além disso, o controle da inflamação das vias aéreas superiores reflete positivamente na melhora dos parâmetros objetivos da função pulmonar.28
 Os CINs na atualidade são considerados a principal forma de tratamento da RA e o tratamento de primeira linha em pacientes com rinite moderada a grave pela maior eficácia nesses pacientes.29
Os CINs na atualidade são considerados a principal forma de tratamento da RA e o tratamento de primeira linha em pacientes com rinite moderada a grave pela maior eficácia nesses pacientes.29
Os CINs apresentam ação anti-inflamatória potente, reduzindo a infiltração inflamatória que ocorre na mucosa nasal, reduzindo os sintomas locais de rinorreia, prurido, obstrução, espirros e hipersecreção. O seu início de ação ocorre em poucas horas, entretanto sua efetiva ação pode se desenvolver após dias ou mesmo semanas.29 Apresentam biodisponibilidade sistêmica mínima, sendo rapidamente eliminado.
Os efeitos colaterais são poucos, estando relacionados à longa duração de tratamento, sendo os mais relatados a ulceração nasal e a epistaxe que pode ser evitada pela correta aplicação do dispositivo de inalação. Não se deve direcionar o aplicador ao septo nasal. Outros efeitos adversos incluem nasofaringite, queimação, irritação e ressecamento.30 Tratamento com doses maiores do que as recomendadas de corticoides nasais podem resultar em supressão adrenal clinicamente significante.
Como a histamina é um mediador presente nas secreções de pacientes com rinite alérgica, os antagonistas H1 orais (AHO) têm um lugar estabelecido e valorizado no tratamento sintomático de reações de hipersensibilidade imediata. Os anti-histamínicos são particularmente eficazes em relação ao prurido, aos espirros e à rinorreia, com pouca atuação na obstrução nasal.
Os anti-histamínicos de segunda geração são preferidos devido aos menores efeitos anticolinérgicos no sistema nervoso central por causarem menos sedação. O início da ação ocorre em até uma hora para a maioria dos agentes, e os níveis séricos máximos são atingidos em duas a três horas. Pacientes em monoterapia com AHO evidenciam um nível de controle inferior ao daqueles que utilizam ClN,24,25 não havendo indicação para pacientes com rinite moderada a grave em que há forte componente inflamatório. Os anti-histamínicos intranasais (AHINs) têm eficácia similar aos compostos orais, porém apresentam início de ação mais rápido e com maior efetividade no controle da obstrução nasal. Entretanto, alguns pacientes se queixam entretanto, de seu sabor amargo.31
A combinação de anti-histamínicos intranasais e corticoides intranasais (AHINs + CINs) é mais eficaz do que isoladamente, principalmente em pacientes com doença moderada a grave.29 Por outro, lado a combinação de AHO com CINs não resultou mais eficaz do que o uso isolado de corticoides intranasais. O achado clássico é a combinação cloridrato de azelastina + propionato de fluticasona (spray intranasal). A base fisiopatológica da superioridade da combinação envolve as duas fases inflamatórias principais da rinite alérgica: 1) Fase imediata que ocorre em minutos caracterizada por liberação de histamina, leucotrienos, prostaglandinas e por ativação mastocitária. Nesta predominam os sintomas de espirros, prurido nasal e rinorreia onde o anti-histamínico intranasal atua rapidamente. 2) Fase tardia que transcorre entre 4 e 24 h, predominando infiltração eosinofílica, citocinas Th2 com inflamação mucosa persistente. Predominam a congestão e obstrução persistentes. Nesta fase o corticoide intranasal é mais eficaz.
Estudos mostram que o anti-histamínico intranasal (principalmente azelastina) apresenta propriedades adicionais, ou seja: efeito anti-inflamatório direto, redução na produção de IL-6, IL-8 e TNF-α, estabilização mastocitária, e redução da hiper-responsividade nasal. A maior evidência se traduz pela melhora 30-40% no escore de sintomas nasais totais, comparado ao corticoide isolado. Estudos celulares em mastócitos cultivados evidenciaram que a azelastina inibiu a ativação e liberação de histamina, reduzindo IL-6 e triptase.32 Revisões farmacológicas mostram que a azelastina bloqueia canais de cálcio dependentes de voltagem, reduz a desgranulação de mastócitos, estabilizando-os, impedindo a liberação de mediadores inflamatórios como leucotrienos e TNF-α. Esse mecanismo explica o efeito mais amplo do medicamento na fase tardia da rinite alérgica.33
A combinação cloridrato de azelastina + propionato de fluticasona intranasal atua em múltiplos níveis da inflamação alérgica (Tabela 1).
Tabela 1 – Mecanismo de Ação da Combinação Cl. de Azelastina + Propionato de Fluticasona
Mecanismo |
Azelastina |
|
Fase Imediata |
bloqueio H1 |
efeito menor |
Mastócitos |
⇓ desgranulação |
estabilização indireta |
Citocinas |
⇓ IL-6, TNF-α |
⇓ transcrição gênica |
Eosinófilos |
efeito modesto |
forte inibição |
Fase tardia |
parcial |
principal ação |
Os estudos ARIA de mundo real registram que muitos pacientes usam corticoide intranasal de forma irregular, enquanto que a combinação tende a ser utilizada sob demanda, mantendo o controle melhor dos sintomas. Isto ocorre provavelmente pelo início de ação mais rápida.24,34
Finalizando: As recomendações baseadas no sistema GRADE para manejo da rinite alérgica, juntamente com a classificação terapêutica proposta pela ARIA e reforçadas por evidências condicionais e dados do mundo real, sustentam a abordagem atualmente adotada. De acordo com essas diretizes, a combinação de anti-histamínicos orais com corticoides intranasais não apresenta superioridade em relação ao uso isolado dos corticoides intranasais. Por outro lado, a associação de anti-histamínícos H1 intranasais com corticoides intranasais demonstra maior eficácia clínica quando comparada ao uso exclusivo dos corticoides intranasais. Além disso, os anti-histamínicos H1 intranasais possuem início de ação rápida, proporcionando alívio dos sintomas em poucos minutos.
Apesar de todo o conhecimento do qual dispomos na atualidade sobre a asma e a rinite, e o conceito de via aérea única, sabemos que a quantidade de corticoide que chega aos pulmões vinda do nariz é insignificante para tratar a asma. Da mesma forma, o corticoide inalatório, apesar de uma parte ficar na orofaringe, deposita-se majoritariamente nos pulmões e não atinge a mucosa nasal em concentração terapêutica para tratar a rinite. O objetivo do tratamento moderno da asma e rinite é usar a menor dose eficaz de corticoide, aplicada diretamente no local da inflamação. Isso maximiza a eficácia e minimiza os efeitos adversos sistêmicos (que ocorreriam se a medicação fosse aplicada por via oral, por exemplo).