| Asma
TRATAMENTO DA ASMA
OMALIZUMABE NA ASMA
Desde que a IgE foi identificada em 1968 como o anticorpo responsável pela reação alérgica do tipo I, a redução de seus níveis passou a ser um importante alvo para o tratamento das doenças alérgicas. Os mecanismos pelos quais a IgE atua ainda não foram totalmente elucidados. Dependem, entretanto, de sua ligação aos receptores de alta afinidade FceRI em mastócitos e basófilos e, talvez, nos receptores de baixa afinidade FceRII em macrófagos, células dendríticas, linfócitos B e outras células como as plaquetas.
O tratamento pelo Omalizumabe foi aprovado pela
Food and Drug Administration (FDA) dos EUA em junho de 2003 e atualmente a GINA preconiza seu uso para pacientes com idade ≥ 6 anos com asma alérgica severa. Também pode ser indicado para pólipos nasais, urticária crônica espontânea (idiopática) e alergia alimentar mediada por IgE.1,2
Grande parte das investigações para o desenvolvimento de uma terapêutica anti-IgE em humanos foi desenvolvida em animais de laboratório. Há mais de quatro décadas, detectou-se em murinos que recebiam anticorpos policlonais IgE derivados do coelho, uma importante redução nos níveis plasmáticos de IgE, bem como supressão no número de linfócitos B geradores deste tipo de imunoglobulina. O tratamento de camundongos com uma simples injeção de anticorpo monoclonal anti-IgE (mAb sigla em inglês de monoclonal antibody) anafilactogênico durante imunização primária reduzia os níveis séricos de IgE, que persistiam baixos por período superior a dois meses, mesmo quando os animais eram expostos ao antígeno, de forma sistemática semanalmente.3 Estes
anticorpos monoclonais murinos (AcMm)
não interferiam, entretanto, na produção de IgM, IgG e IgA pelas células B.
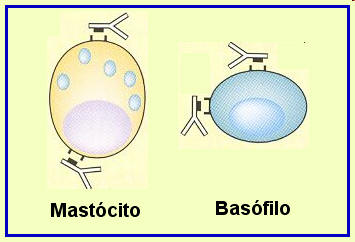 Com o desenvolvimento de técnicas para produzir anticorpos monoclonais, desenvolveu-se um AcMm não anafilactogênico que reconhece o mesmo sítio de ligação do receptor de alta afinidade FceRI da IgE livre (porção Fc específica – Cε3), bloqueando-o e prevenindo a liberação de mediadores inflamatórios por mastócitos e basófilos. Este anticorpo forma complexos seletivos com a IgE livre, porém não com a IgG ou IgA. Um importante aspecto deste composto constituía-se no fato de estes anticorpos não se ligarem à IgE previamente acoplada aos receptores FceRI, nem aos receptores de baixa afinidade FceRII ou CD23, porque o epítopo da IgE contra o qual eles eram dirigidos já se encontrava ocupado, evitando-se desta forma a ativação celular de mastócitos e basófilos (Figura 1).3 Com o desenvolvimento de técnicas para produzir anticorpos monoclonais, desenvolveu-se um AcMm não anafilactogênico que reconhece o mesmo sítio de ligação do receptor de alta afinidade FceRI da IgE livre (porção Fc específica – Cε3), bloqueando-o e prevenindo a liberação de mediadores inflamatórios por mastócitos e basófilos. Este anticorpo forma complexos seletivos com a IgE livre, porém não com a IgG ou IgA. Um importante aspecto deste composto constituía-se no fato de estes anticorpos não se ligarem à IgE previamente acoplada aos receptores FceRI, nem aos receptores de baixa afinidade FceRII ou CD23, porque o epítopo da IgE contra o qual eles eram dirigidos já se encontrava ocupado, evitando-se desta forma a ativação celular de mastócitos e basófilos (Figura 1).3
A utilização no homem do AcMm ficou limitada pela ocorrência da xenogênese, com formação de anticorpos depois de repetidas administrações. Esta resposta antigênica reduz a eficácia destes anticorpos pela diminuição de suas meias-vidas através da formação de complexos anticorpos-antianticorpos, determinando reações anafiláticas.
Para fins de aplicação clínica, os anticorpos monoclonais derivados de murinos foram humanizados. O omalizumabe (rhuMAb-E-25) é um anticorpo monoclonal recombinante humanizado. Os resíduos de aminoácidos da região variável da imunoglobulina do camundongo que se ligam à IgE foram enxertados na região constante da IgG1 humana, resultando em uma nova proteína/imunoglobulina com características humanas > 95% (IgG1-k), minimizando os riscos de reações imunes, pois apenas três resíduos de aminoácidos do omalizumabe estão ausentes no conjunto de anticorpos humanos.
Sumarizando, este processo envolve a remoção da porção imunogênica do anticorpo IgG murino, inserindo-se em seu lugar uma porção de IgG1 humana correspondente. O omalizumabe se liga à IgE livre circulante e forma pequenos complexos triméricos ou hexaméricos (Figura2).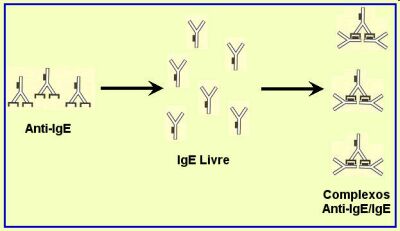
Após a sua aplicação subcutânea ou intravenosa, os níveis séricos da IgE livre caem rapidamente (>99%), através de uma ação dose-dependente.4 Da mesma forma, ocorre a redução da expressão do receptor de alta afinidade FceRI (96%) e na liberação de histamina antígeno-estimulada pelos basófilos (90%).4 Para a obtenção de eficácia terapêutica, sem a formação de anticorpos anti-IgE anafilactogênicos, deve ser aplicada a maior dose possível que diminua os níveis de IgE. Isto significa que a dosagem anti-IgE necessária deve ser individualizada de acordo com os níveis de IgE total de cada paciente, objetivando-se a obtenção de níveis de IgE indetectáveis durante todo o tratamento (redução > 95% da IgE livre), sem o qual não haverá o efeito esperado.3,5
Omalizumabe é um anticorpo monoclonal IgG1 humanizado derivado de DNA recombinante contra IgE. Liga-se à IgE circulante livre no domínio Cε3, o mesmo ponto que a IgE normalmente se ligaria ao seu receptor de alta afinidade (FceRI) em basófilos, mastócitos e células dendríticas. Como resultado, inibe a resposta mediada por IgE e regula negativamente os receptores de alta afinidade nos mastócitos e basófilos. |
|
A formação dos complexos omalizumabe-IgE acarreta um aumento (dose dependente) de duas a nove vezes nos níveis de complexos anti-IgE/IgE, com consequente desaparecimento da IgE livre circulante.5,6 A análise por ultracentrifugação e cromatografia de exclusão identifica os complexos omalizumabe/IgE (anti-IgE/IgE) como heteroexâmeros com uma massa molecular de um milhão ou menos.7 Como estes complexos não podem se ligar aos receptores IgE, são desprovidos de atividade IgE biológica. Estes complexos são excluídos pela interação com receptores Fcg dos leucócitos e pelo sistema retículo endotelial (SRE).8 A formação do complexo não está associada a anormalidades da função renal ou a outra evidência clínica de doença do complexo imune.9
O omalizumabe previne crises de asma após teste de provocação por inalação de alérgenos, tanto à resposta imediata como à tardia, em pacientes com doença alérgica leve.9,10 Fahy et al.9 avaliaram os efeitos do omalizumabe durante nove semanas em 19 pacientes alérgicos com asma (dois grupos paralelos), através de um estudo randomizado, duplo-cego, placebo-controlado. Obtiveram redução importante na IgE sérica total (p < 0,001, entre os grupos), aumento na dose necessária para provocar uma resposta imediata na asma, acentuada redução na queda do VEF1 (Figura 3), e na eosinofilia.
A
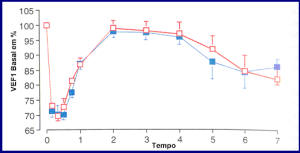 |
B
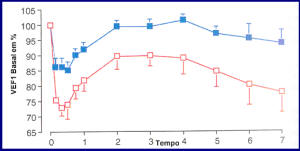 |
Em outra publicação Noga et al.10 avaliaram em um subestudo, os efeitos da droga em 35 pacientes com testes cutâneos positivos (prick test), que faziam uso de corticoide por inalação (500–1.000 mcg) e que participaram de um estudo multicêntrico randomizado, duplo-cego e placebo controlado. O omalizumabe foi administrado a cada quatro semanas. Após 16 semanas obtiveram redução significativa da IL-13 (p< 0,01). A IL-5 e IL-8 diminuíram no grupo do omalizumabe quando comparadas aos valores basais. A liberação da histamina apresentou queda significante (p< 0,01). A resistência das vias aéreas e o teste de provocação com queda de 20% do VEF1 foram medidos antes, após 16 semanas e três meses após o final do protocolo. Ambos os parâmetros tiveram queda expressiva (p< 0,05). Quando comparado ao placebo a contagem dos eosinófilos do sangue periférico foi menor (p< 0,01).
Em vários estudos efetuados,11-15 o omalizumabe demonstrou ser capaz de:
∎ Reduzir as exacerbações da asma mesmo em paciente com doença moderada e severa
∎ Diminuir a eosinofilia
∎ Melhorar a qualidade de vida, com a diminuição dos sintomas
∎ Melhorar os parâmetros das provas de função pulmonar e
∎ Reduzir as doses de corticoides e ß-agonistas
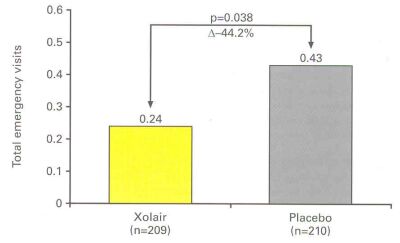 O omalizumabe foi bem tolerado em pacientes adultos e adolescentes, com asma, rinite e outras condições alérgicas16 sendo que destes, 3.700 apresentavam asma de moderada a severa. A eficácia e a tolerabilidade do omalizumabe têm sido bem estudadas em pacientes com asma alérgica severa. O estudo INNOVATE17 que analisou exclusivamente pacientes com asma alérgica grave mal controlada demonstrou a eficácia do omalizumabe nesta população de alto risco com redução de 50% nas exacerbações severas e diminuição em 44,2% nos atendimentos de emergência (Figura 4). O omalizumabe foi bem tolerado em pacientes adultos e adolescentes, com asma, rinite e outras condições alérgicas16 sendo que destes, 3.700 apresentavam asma de moderada a severa. A eficácia e a tolerabilidade do omalizumabe têm sido bem estudadas em pacientes com asma alérgica severa. O estudo INNOVATE17 que analisou exclusivamente pacientes com asma alérgica grave mal controlada demonstrou a eficácia do omalizumabe nesta população de alto risco com redução de 50% nas exacerbações severas e diminuição em 44,2% nos atendimentos de emergência (Figura 4).
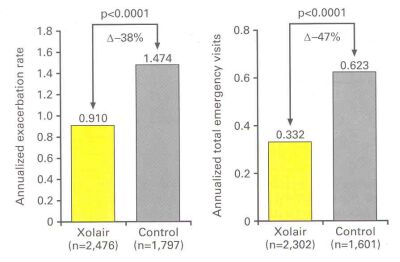 Os resultados de estudo INNOVATE foram confirmados pelos achados da análise de um pool de sete outras experimentações clínicas.18 Destas, cinco eram estudos randomizados, duplo-cego, placebo-controlado, nos quais o paciente recebia omalizumabe ou placebo. Como no INNOVATE, o omalizumabe foi acrescentado à medicação em curso utilizada pelos pacientes. Esta análise demonstrou uma redução nas taxas de exacerbação da asma de 38,3% e de 47% na procura a atendimentos de emergência de pacientes com asma persistente, sendo que 93% de pacientes apresentavam asma persistente severa e 67% eram enquadrados como asma de alto risco para morte. Pacientes que receberam omalizumabe apresentaram uma taxa de exacerbação da asma anualizada de 0,91, enquanto no grupo controle alcançava 1,474 (diferença de tratamento 0,564) p<0,0001 v. controle. (Figura 5). Os resultados de estudo INNOVATE foram confirmados pelos achados da análise de um pool de sete outras experimentações clínicas.18 Destas, cinco eram estudos randomizados, duplo-cego, placebo-controlado, nos quais o paciente recebia omalizumabe ou placebo. Como no INNOVATE, o omalizumabe foi acrescentado à medicação em curso utilizada pelos pacientes. Esta análise demonstrou uma redução nas taxas de exacerbação da asma de 38,3% e de 47% na procura a atendimentos de emergência de pacientes com asma persistente, sendo que 93% de pacientes apresentavam asma persistente severa e 67% eram enquadrados como asma de alto risco para morte. Pacientes que receberam omalizumabe apresentaram uma taxa de exacerbação da asma anualizada de 0,91, enquanto no grupo controle alcançava 1,474 (diferença de tratamento 0,564) p<0,0001 v. controle. (Figura 5).
Normansell et al.19 em
metanálise que incluiu uma revisão de 25 estudos envolvendo 6.382 pacientes concluíram que o omalizumabe foi eficaz na redução das exacerbações e hospitalizações da asma como tratamento adjuvante aos corticoides inalados (CI) e durante as fases de redução dos corticoides dos ensaios clínicos. A droga foi significativamente mais eficaz que o placebo quanto ao número de participantes que foram capazes de reduzir ou retirar seus CIs. O omalizumabe foi geralmente bem tolerado, embora mais reações no local da injeção tenham sido observadas com o omalizumabe.
Mansur et al.20 analisaram os resultados clínicos de longo prazo do tratamento do omalizumabe na asma alérgica grave e observaram redução na admissão hospitalar de 80,7%, enquanto as hospitalizações anuais por paciente foram reduzidas na média de 4,8 para 0,89 pós-omalizumabe (p<0,00001). Houve redução de 76,7% na dose diária de corticoide oral, com dose média de manutenção (equivalente de prednisolona), de 25,8 mg (n = 43) para 6,0 mg (p< 0,0001), associada à melhora clinicamente significante no questionário de controle de asma (ACQ ) do escore médio de 4,1 (intervalo 3,7– 4,7) a 2,27 (intervalo 0,5 – 4,1) (p<0,0001). O percentual médio teórico basal do VEF1 melhorou de 59,2% para 75,7% no decurso do tratamento (p = 0,001).
Outro estudo prospectivo, multicêntrico, de 12 meses, em braço único, com o omalizumabe, o PROSPERO, avaliou um grupo com idade ≥12 anos com asma alérgica eosinofílica no qual foram inscritos 806 pacientes, 801 (99,4%) receberam o medicamento e 622 (77,2%) completaram o estudo. As taxas de exacerbações de asma melhoraram significativamente de 3,00 ± 3,28 nos 12 meses que precederam ao protocolo para valores de 0,78 ± 1,37 (p< 0,001) ao final do estudo. Nos adolescentes houve queda semelhante 2,80 ± 2,64 para 0,46 ± 0,82. Redução de 81,9% no percentual de pacientes com uma ou mais internações foi observada; 22,1% de pacientes relataram uma ou mais hospitalizações nos 12 meses que antecederam o estudo versus 4,0% durante o ensaio clínico. No estudo PROSPERO, eventos anafiláticos foram relatados em apenas três pacientes (0,4%) de gravidade moderada, todos em adultos. Não foram relatados eventos na população adolescente.21
Análises post hoc de um grande estudo longitudinal – EXTRA – (n = 850) em pacientes com asma alérgica grave não controlada estudaram três biomarcadores da inflamação Th2 como preditores de resposta ao omalizumabe. As diferenças na frequência de exacerbação entre omalizumabe e placebo foram maiores nos grupos com alta contagem de eosinófilos,
concentração fracionada de óxido nítrico exalado (FeNO) alta e elevada periostina sérica.22
Com mais de 2,25 milhões de pacientes-anos de exposição, o omalizumabe demonstrou eficácia e boa tolerabilidade no tratamento da asma moderada a grave em adultos e crianças.19,23,24 Dois estudos destacam seus benefícios em populações pediátricas urbanas: o estudo ICATA (Inner-City Anti-IgE Therapy for Asthma)25 que durante um ano avaliou sua eficácia em crianças, adolescentes e jovens adultos com asma persistente. Já O estudo PROSE (Preventative Omalizumab or Step-Up Therapy for Fall Exacerbations) enfatizou o período de retorno às aulas no outono, para melhor avaliar as crianças com asma alérgica, quando de exacerbações.26 Em ambos, o omalizumabe obteve controle da asma e redução das exacerbações, atuando preventivamente contra a ativação de mastócitos e modificando a ação da IgE quanto às propriedades antivirais.25,26
O omalizumabe está indicado para a asma alérgica,
rinossinusite crônica com pólipo nasal (RSCcPN)
e também no tratamento da urticária crônica idiopática
(UCI). Na asma o omalizumabe é aplicado por via SC nas doses de 75 a 375 mg a cada 2 ou 4 semanas. Não há opções de dosagem para indivíduos >150 kg. Determina-se a dose (mg) e frequência de dosagem a partir do nível sérico de IgE total (UI/ml), medido antes do início do tratamento e pelo peso corporal (kg). Veja as tabelas de determinação de doses e número de fraccionamento de injeções. (Tabelas 1, 2 e 3) Na UCI as doses oscilam entre 150 ou 300 mg SC a cada 4 semanas e não dependem do nível sérico de IgE ou do peso corporal.
Na RSCcPN o omalizumabe está indicado nas doses de 75 a 600 mg a cada 2 a 4 semanas por via SC. Determinar a dose (mg) e frequência de dosagem através do nível sérico de IgE total (UI/ml) obtido antes do início do tratamento assim como o peso coporal (kg). Veja em tabela própria de determinação de doses, não disponibilizada nesta sessão.
Estas doses são baseadas na quantidade estimada de droga que é necessária para reduzir os níveis de IgE livre circulante para menos de 10 UI/ml. A meia-vida de eliminação é de 1–4 semanas. A via de administração é a subcutânea, preconizando-se que as primeiras doses sejam aplicadas por um profissional da área de saúde capaz de gerenciar possível anafilaxia. Como a solução injetável é levemente viscosa, o tempo de aplicação demora de 5–10 segundos. Doses maiores de 150 mg deverão ser divididas, não devendo ser ultrapassado este valor por local de aplicação (Tabela 3). Admite-se seu uso em crianças a partir de ≥ 6 anos de idade.
Não está indicada a monitorização dos níveis da IgE total durante o curso do tratamento com o omalizumabe, pois estes estarão sempre elevados como resultado da presença de complexos circulantes IgE-anti-IgE.
Um método de investigação para quantificar a IgE livre do soro foi apresentado e poderá constituir-se em uma nova opção para monitorizar o tratamento com omalizumabe.
Normalmente é administrado por 3 a 6 meses antes de se poder avaliar a resposta.28 Dados da literatura enfatizam que os pacientes devem ser tratados por pelo menos 16 semanas para que se possa avaliar com segurança os efeitos da droga. Nestes, tratados por 16 semanas, 87% obtiveram resposta ao nível da 12ª semana.29 Na prática, avaliamos a resposta ao longo de 12 meses. Alguns pacientes respondem por longo prazo.27
A razão pela qual alguns pacientes com asma alérgica grave respondem ao omalizumabe e outros não pode estar relacionada à magnitude em que o bloqueio da ligação da IgE aos mastócitos e células dendríticas produz uma regulação negativa aos receptores de alta afinidade – FceRI.30
Algumas considerações sobre o tratamento com omalizumabe:
➢ Os não respondedores devem ser reconhecidos o mais cedo possível e o tratamento deve ser descontinuado. Propõe-se que, se não houver resposta clínica após um ciclo de 4 meses da medicação, este deve ser descontinuado, pois a administração adicional de omalizumabe não será benéfica.31
➢ A elevação combinada dos biomarcadores Th2 (níveis séricos de eosinófilos ≥ 260 por µL, FeNO exalado ≥ 24 ppb ou nível de periostina ≥ 53 ng ml-1) anteveem uma melhor resposta ao omalizumabe.32
➢ De acordo com as evidências mais recentes, a eficácia do omalizumabe independe dos níveis séricos de eosinófilos no sangue periférico.33,34
➢ A dose deve ser mantida no decurso de todo o tratamento. Na eventualidade de ocorrer perda ponderal maior do que 10%, em curto espaço de tempo, a dose deverá ser revista.
➢ Mesmo com o sucesso a longo prazo do tratamento bem-sucedido com o omalizumabe, a descontinuação geralmente resulta na recorrência da doença.35
Quanto aos efeitos adversos, os mais descritos são: reações no local da injeção, febre, infecção viral, infecção do trato respiratório superior, sinusite, cefaleia, faringite, dor abdominal, artralgias, fadiga, rash cutâneo e urticária. Os efeitos adversos mais graves relatados são: angiíte granulomatosa alérgica (S. Churg-Strauss), trombocitopenia idiopática grave e doença do soro.
A IgE é classicamente o anticorpo primário no combate às infecções parasitárias. Há preocupações de que o tratamento com omalizumabe coloque os pacientes em risco aumentado de infecções por helmintos e alguns dados demonstram que em áreas onde há um risco aumentado de infecção por helmintos, como em regiões tropicais e intertropicais, onde a prevalência é alta (às vezes > 40%) o tratamento com omalizumabe aumenta levemente o risco dos pacientes em comparação com o placebo.36
Os efeitos mais sérios são a anafilaxia (angioedema, broncospasmo alérgico, ...) e a manifestação de doenças malignas. A anafilaxia ocorre dentro de duas horas após a primeira aplicação ou dose subsequente em < 0,1% dos pacientes, sem qualquer outro desencadeante alérgico identificável. Sempre que ocorrer reação severa de hipersensibilidade, o tratamento deverá ser suspenso definitivamente. O impacto da longa exposição ao omalizumabe e o risco de malignização são desconhecidos. O estudo epidemiológico EXCELS avaliou a incidência de malignidade em pacientes com asma moderada a grave tratados com ou sem omalizumabe e avaliou a segurança em longo prazo da droga em um ambiente de prática clínica, sendo que os resultados sugerem que o tratamento com o omalizumabe não está associado a um risco aumentado de malignidade.37
Omalizumabe na Gravidez
Vários relatos de casos foram publicados sobre sua eficácia e segurança em mulheres grávidas com urticária crônica idiopática.38
O estudo observacional do uso e segurança de Xolair (omalizumabe) durante a gravidez (EXPECT) foi um estudo prospectivo estabelecido entre 2006 e 2018 para avaliar os resultados perinatais em 250 mulheres grávidas expostas ao omalizumabe e seus bebês. A coorte de comparação foi criada tomando como base bancos de dados de saúde em Quebec, Canadá, de 1153 mulheres grávidas com asma moderada a grave, sem exposição ao omalizumabe. Os autores concluíram que não detectaram evidências de um risco aumentado de anomalias congênitas importantes no grupo tratado com a medicação biológica.39
Tabelas:
Tabela 1 — Doses Subcutâneas de Omalizumabe a Cada 2 ou 4 Semanas para Pacientes com Asma de 12 Anos de Idade ou Mais
IgE Sérica (UI/ml) Pré-tratamento
|
Frequência de Dosagem
|
Peso Corporal (kg) |
30-60 kg |
>60-70 kg |
>70-90 kg |
> 90-150 kg |
| |
|
Dose (mg) |
≥30-100 |
Quatro Semanas |
150 |
150 |
150 |
300 |
>100-200 |
300 |
300 |
300 |
225 |
>200-300 |
300 |
225 |
225 |
300 |
-300-400 |
Duas Semanas |
225 |
225 |
300 |
|
>400-500 |
300 |
300 |
375 |
>500-600 |
300 |
375 |
Dados Insuficientes |
>600-700 |
375 |
para Recomendar uma Dose
|
Tabela 2 — Doses Subcutâneas de Omalizumabe a Cada 2 ou 4 Semanas para Pacientes Pediátricos com Asma que Começam o Omalizumabe Entre as Idades de 6 a < 12 Anos
 
Tabela 3 — Conversão de Dose Para Número de Frascos-Ampola, Número de Injeções e Volume Total de Injeção para Cada Administração. 1,2 ml = Volume Máximo Fornecido por Frasco-Ampola (Xolair150 mg)
Dose |
Nº de Frascos-ampola |
Nº de injeções |
VolumeTotal de Injeção |
75 mg |
1 |
1 |
0,6 ml |
150 mg |
1 |
1 |
1,2 ml |
225 mg |
2 |
2 |
1,8 ml |
300 mg |
2 |
2 |
2,4 ml |
375 mg |
3 |
3 |
3,0 ml |
450 mg |
3 |
3 |
3,6 ml |
525 mg |
4 |
4 |
4,2 ml |
600 mg |
4 |
4 |
4,8 ml |
1,2 ml - volume máximo fornecido por frasco-ampola (Xolair ®150 mg)
|
Outra questão discutida quanto à segurança do uso da droga relaciona-se com a possibilidade do desencadeamento de doenças do complexo imune pelo tratamento anti-IgE. Devido à humanização do anticorpo e ao pequeno tamanho dos complexos anti-IgE/IgE, espera-se prevenir e resposta imune. É importante salientar que o tamanho máximo dos complexos imunes gerados in vitro e in vivo do omalizumabe tem sido constituído por duas ou três moléculas de IgE com duas ou três moléculas anti-IgE. Este tamanho corresponde ao da IgM humana, e tais complexos são incapazes de ativar o complemento.
ABPA
A utilização do omalizumabe na aspergilose broncopulmonar alérgica (ABPA)
foi inicialmente avaliada por Tillie-Leblond et al.40 que realizaram um estudo de braço único durante um ano em 16 casos com ABPA, quando obtiveram redução significativa da taxa de exacerbação e da necessidade de corticoides sistêmicos. Voskamp et al.41 realizaram um estudo randomizado, duplo-cego, placebo controlado, de quatro meses de duração. Após um período de washout, treze pacientes com asma e ABPA foram identificados e receberam 375 mg de omalizumabe a cada 2 semanas por 4 meses. Quando comparado ao grupo placebo as exacerbações de ABPA ocorreram em menor frequência durante o tratamento com omalizumabe 2 vs. 12 eventos. A fração exalada do óxido nítrico (FeNO ) teve queda de 30,5 para 17,1 ppb após o tratamento com a droga, mas sem repercussão na função pulmonar. Atualmente a dose preconizada é baseada no peso corporal e nos valores séricos de IgE total, não excedendo 375 mg por injeção subcutânea duas vezes por mês, para pacientes refratários ou intolerantes à primeira linha de tratamento.
A maioria dos pacientes com ABPA apresenta níveis basais de IgE superiores a 1.000 UI/mL, frequentemente ultrapassando o limite da faixa de medição disponível nas tabelas de dosagem. Consequentemente, os parâmetros atuais para o cálculo da dose de omalizumabe muitas vezes se mostram insuficientes na prática clínica, resultando em uma dosagem subótima devido aos níveis significativamente elevados de IgE, característicos dessa condição. No entanto, um estudo randomizado e controlado por placebo demonstrou que, apesar dos altos níveis de IgE em pacientes com ABPA, a dose de rotina de omalizumabe (375 mg a cada 2 semanas como injeção subcutânea) pode ser suficiente para provocar benefícios clínicos e imunológicos nesses pacientes.41
Referências
01.Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention, 2025.
Updated May 2025. Disponível em: www.ginasthma.org
02.Rodrigo GJ, Neffen H. Systematic review on the use of omalizumab for treatment of astmatic children and adolescentes. Pediatr Allergy Immunol 2015; 26:551-6.
03.Arshad SH, Babu KS, Holgate ST. Anti-IgE therapy in asthma and allergy. London: Martin Dunitz; 2001.
04.MacGlashan DW Jr, Bochner BS, Adelman DC, Jardieu PM, Togias A, McKenzie-White J, Sterbinsky SA, Hamilton RG, Lichtenstein LM.
Down-regulation of FceRI expression on human basophils during in vivo treatment of atopic patients with anti-IgE antibody. J Immunol 1997; 158:1438-45.
05.Casale TB, Bernstein IL, Busse WW, LaForce CF, Tinkelman DG, Stoltz RR, Dockhorn RJ, Reimann J, Su JQ, Fick RB Jr, Adelman DC.
Use of an anti-IgE humanized monoclonal antibody in ragweed-induced allergic rhinitis. J Allergy Clin Immunol 1997; 100:110-21.
06.Schoenhoff M, Bates D, Ruppel J, et al. Pharmacokinetics/dynamics following administration of a recombinant humanized monoclonal anti-IgE antibody in the cromolgus monkey [abstract]. J Allergy Clin Immunol 1995; 95:356.
07.Liu J, Lester P, Builder S, Shire SJ. Characterization of complex formation by humanized anti-IgE monoclonal antibody and monoclonal human IgE. Biochemistry 1995; 34:10474-82.
08.Fox JA, Hotaling TE, Struble C, Ruppel J, Bates DJ, Schoenhoff MB. Tissue distribution and complex formation with IgE of an anti-IgE antibody after intravenous administration in cynomolugus monkeys. J Pharmacol Exp Ther 1996; 279:1000-8.
09.Fahy JV, Fleming HE, Wong HH, et al. The effects of anti-IgE monoclonal antibody on the early-and late-phase responses to allergen inhalation in asthmatic subjects. Am J Respir Crit Care Med 1997; 155:1828-34.
10.Noga O, Hanf G, Kunkel G. Immunological and clinical changes in allergic asthmatics following treatment with omalizumab. Inter Arch Allergy Immunol 2003; 131:46-52.
11.Boulet LP, Chapman KR, Côté J, Kalra S, Bhagat R, Swystun VA, Laviolette M, Cleland LD, Deschesnes F, Su JQ, DeVault A, Fick RB Jr, Cockcroft DW. Inhibitory effects of an anti-IgE antibody E25 on allergen-induced early asthmatic response. Am J Respir Crit Care Med 1997; 155:1835-40.
12.Fick RB, Rohane PW, Gupta N et al. Anti-inflammatory effects of a recombinant monoclonal anti-IgE (E25) in asthma. Am J Respir Crit Care Med 2000; 161:A199.
13.Busse WW, Fahy JV, Fick RB. A pilot study of the effects of an anti-IgE antibody (E25) on airway inflammation in moderate-severe asthma. Am J Respir Crit Care Med 1998; 157:A456.
14.Milgrom H, Fick RB Jr, Su JQ, Reimann JD, Bush RK, Watrous ML, Metzger WJ.
Treatment of allergic asthma with monoclonal anti-IgE antibody. N Engl J Med 1999; 341:1966-73.
15.Lemanske RF; Nayak A; McAlary M; Everhard F; Fowler-Taylor A; Gupta N. Omalizumab improves asthma-related quality of life in children with allergic asthma. Pediatrics; 110:E55.
16.Corren J, Casale T, Lanier BQ. Omalizumab is well tolerated in adolescent/adult patients (>12 years) with moderate-to-severe asthma. J Allergy Clin Immunol 2005; 115:S75.
17.Humbert M, Beasley R, Ayres J, Slavin R, Hébert J, Bousquet J, Beeh KM, Ramos S, Canonica GW, Hedgecock S, Fox H, Blogg M, Surrey K. Benefits of omalizumab as add-on therapy in patients with severe persistent asthma who are inadequately controlled despite best available therapy (GINA 2002 step 4 treatment): INNOVATE. Allergy 2005; 60:309-16.
18.Bousquet J, Cabrera P, Berkman N, Buhl R, Holgate S, Wenzel S, Fox H, Hedgecock S, Blogg M, Cioppa GD.
The effect of treatment with omalizumab, an anti-IgE antibody, on asthma exacerbations and emergency medical visits in patients with severe persistent asthma. Allergy 2005; 60:302-8.
19.Normansell R, Walker S, Milan SJ, Walters EH, Nair P. Omalizumab for asthma in adults and children. Cochrane Database Syst Reviews 2014, Issue 1. Art. No.: CD003559.DOI: 10.1002/14651858.CD003559.pub4.
20.Mansur AH, Srivastava S, Mitchell V, Sullivan J, Kasujee L. Longterm clinical outcomes of omalizumab therapy in severe allergic asthma: Study of efficacy and safety. Respir Med 2017; 124:36-43.
21.Casale TB, Luskin AT, Busse W, Zeiger RS, Trzaskoma B, Yang M, Griffin NM, Chipps BE. Omalizumab effectiveness by biomarker status in patients with asthma: evidence from PROSPERO, a prospective real-world study. J Allergy Clin Immunol Pract. 2019; 7:156-164.
22.Hanania NA, Wenzel S, Rosén K, et al. Exploring the effects of omalizumab in allergic asthma: an analysis of biomarkers in the EXTRA study. Am J Respir Crit Care Med. 2013; 187:804-811.
23.Novartis. Data on file, (2024).
24.Domingo C, Busse WW, Hanania NA, Ertugrul M, Millette LA, Maio-Twofoot T, Jaumont X, Palomares O. The Direct and Indirect Role of IgE on Airway Epithelium in Asthma. Allergy 2025; 80:919-931.
25.Busse WW, Morgan WJ, Gergen PJ, Mitchell HE, Gern JE, Liu AH, Gruchalla RS, Kattan M, Teach SJ, Pongracic JA, Chmiel JF, Steinbach SF, Calatroni A, Togias A, Thompson KM, Szefler SJ, Sorkness CA. Randomized trial of omalizumab (anti-IgE) for asthma in inner-city children. N Engl J Med 2011; 364:1005-15.
26.Teach SJ, Gill MA, Togias A, Sorkness CA, Arbes SJ Jr, Calatroni A, Wildfire JJ, Gergen PJ, Cohen RT, Pongracic JA, Kercsmar CM, Khurana Hershey GK, Gruchalla RS, Liu AH, Zoratti EM, Kattan M, Grindle KA, Gern JE, Busse WW, Szefler SJ. Preseasonal treatment with either omalizumab or an inhaled corticosteroid boost to prevent fall asthma exacerbations. J Allergy Clin Immunol 2015; 136:1476-1485.
27.Hamilton RG, Marcotte GV, Saini SS. Immunological methods for quantifying free and total serum IgE levels in allergy patients receiving omalizumab (Xolair) therapy. J Immunol Methods 2005; 303:81-91.
28.Chang TW. The pharmacological basis of anti-IgE therapy. Nat Biotechnol 2000; 18:157-62.
29.Easthope S, Jarvis B. Omalizumab. Drugs 2001; 61:253-60.
30.Cho SH, Seo JY, Choi DC, Yoon HJ, Cho YJ, Min KU, Lee GK, Seo JW, Kim YY. Pathological changes according to the severity of asthma. Clin Exp Allergy 1996; 26:1210-9.
31.Bousquet J, Wenzel S, Holgate S, Lumry W, Freeman P, Fox H. Predicting response to omalizumab, an anti-IgE antibody, in patients with allergic asthma. Chest 2004; 125:1378-86.
32.Chung KF, Wenzel SE, Brozek JL, Bush A, Castro M, Sterk PJ, Adcock IM, Bateman ED, Bel EH, Bleecker ER, Boulet LP, Brightling C, Chanez P, Dahlen SE, Djukanovic R, Frey U, Gaga M, Gibson P, Hamid Q, Jajour NN, Mauad T, Sorkness RL, Teague WG.
International ERS/ATS guidelines on definition, evaluation and treatment of severe asthma. Eur Respir J 2014; 43:343373.
33.Humbert M, Taille C, Mala L, Le Gros V, Just J, Molimard M. Omalizumab effectiviness in patients with severe allergic asthma according to blood eosinophil count: the STELLAR study. Eur Respir J 2018;51:
1702523.
34.Caminati M, Vianello A, Chieco Bianchi F, Festi G, Guarnieri G, Marchi MR, Micheletto C, Olivieri M, Tognella S, Guerriero M, Senna G; NEONET Study Group. Relevance of TH2 Markers in the Assessment and Therapeutic Management of Severe Allergic Asthma: A Real-Life Perspective. J Investig Allergol Clin Immunol . 2020; 30:35-41.
35.Molimard M, Mala L, Bourdeix I, Le Gros V. Observational study in severe asthmatic patients after discontinuation of omalizumab for good asthma control. Respir Med 2014; 108:571-576.
36.Cruz AA, Lima F, Sarinho E, Ayre G, Martin C, Fox H, Cooper PJ. Safety of anti-immunoglobulin E therapy with omazilumab in allergic patients at risk of geohelmintth infection. Clin Exp Allergy 2007; 37:197-207.
37.Long A, Rahmaoui A, Rothman KJ, Guinan E, Eisner M, Bradley MS, Iribarren C, Chen H, Carrigan G, Rosén K, Szefler SJ. Incidence of malignancy in patients with moderate-to-severe asthma treated with or without omalizumab. J Allergy Clin Immunol 2014; 134:560-567.
38.Cuervo-Pardo L, Barcena-Blanch M, Radojicic C. Omalizumab use during pregnancy for CIU: a tertiary care experience. Eur Ann Allergy Clin Immunol 2016 Jul; 48:145-6.
39.Namazy JA, Blais L, Andrews EB, Scheuerle AE, Cabana MD, Thorp JM, Umetsu DT, Veith JH, Sun D, Kaufman DG, Covington DL, Mukhopadhyay S, Fogel RB, Lopez-Leon S, Spain CV. Pregnancy outcomes in the omalizumab pregnancy registry and a disease-matched comparator cohort. J Allergy Clin Immunol 2020 Feb; 145:528-36.
40.Tillie-Leblond I, Germaud P, Leroyer C, Tétu L, Girard F, Devouassoux G, Grignet JP, Prudhomme A, Dusser D, Wallaert B. Allergic bronchopulmonary aspergillosis and Omalizumab. Allergy 2011; 66:1254-6.
41.Voskamp AL, Gillman A, Symons K, Sandrini A, Rolland JM, O'Hehir RE, Douglass JA. Clinical efficacy and immunologic effects of omalizumab in allergic bronchopulmonary aspergillosis. J Allergy Clin Immunol Pract 2015; 3:192199.
| |
Home
Design by Walter Serralheiro |
|
|